चतुष्फलकीय रिक्ति , अष्टफलकीय रिक्ति , चतुष्फलकीय रिक्तियाँ , अष्ट फलकीय रिक्तियां Tetrahedral voids in hindi
tetrahedral and octahedral voids in hindi difference चतुष्फलकीय रिक्ति , अष्टफलकीय रिक्ति , चतुष्फलकीय रिक्तियाँ , अष्ट फलकीय रिक्तियां क्या है ?
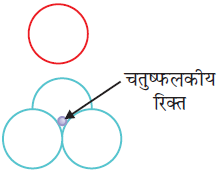
1. एक परत पर दूसरी परत रखना : इस संकुलन में द्विविमीय षट्कोणीय निबिड़तम संकुलित प्रथम परत पर दूसरी परत को इस प्रकार से रखते है कि दूसरी परत के गोले प्रथम परत के अवनमनों में समा जाए , इस प्रकार इसमें दो तरह की रिक्तियों का निर्माण होता है –
दूसरी परत पर तीसरी परत को रखना : अवयवी गोलों की दूसरी पर जब तीसरी परत को रखा जाता है तो इसमें चतुष्फलकीय रिक्ति या अष्टफलकीय रिक्तियों का आसादन (ढक दिया जाता है ) हो जाता है।
अत: इसमें दो संभावनाएं बनती है –
(A) चतुष्फलकीयरिक्तियों का आसादन : चतुष्फलकीय रिक्ति के आसादन से षट्कोणीय निबिड़तम संकुल (HCP) का निर्माण होता है , इस व्यवस्था में अवयवी गोलों की प्रथम परत तीसरी परत के साथ तथा दूसरी पर चौथी परत के साथ समानता रखती है इसे ABAB परतीय व्यवस्था भी कहते है , इस व्यवस्था में उपसहसंयोजन संख्या 12 व संकुलन क्षमता 74% होती है।
जिंक व मैग्नीशियम में ऐसी व्यवस्था पायी जाती है।
(B) अष्टफलकीय रिक्तियों का आच्छादन : अष्टफलकीय रिक्तियों के आच्छादन से घनीय निबिड़तम संकुलन (CPP) का निर्माण होता है , इस व्यवस्था में अवयवी गोलों की प्रथम परत चौथी परत के साथ तथा दूसरी परत पाँचवी परत के साथ एवं तीसरी परत छट्ठी परत के साथ समानता रखती है इसे ABC ABC परतीय व्यवस्था में कहते है , इस व्यवस्था में उपसहसंयोजन संख्या 12 तथा संकुलन क्षमता 74% होती है।
उदाहरण : Ag व Cu में इस प्रकार की व्यवस्था पायी जाती है।
प्रश्न : षट्कोणीय निबिड़तम संकुलन (HCP) व घनीय निबिड़तम संकुलन (CCP) में अंतर लिखिए।
उत्तर :
|
षट्कोणीय निबिड़ संकुलन (HCP)
|
घनीय निबिड़तम संकुलन (CCP)
|
|
1. यह संकुलन चतुष्फलकीय रिक्तियों के आच्छादन से बनता है।
|
यह संकुलन अष्टफलकीय रिक्तियों के आच्छादन से बनता है। |
|
2. इसमें ABAB परतीय व्यवस्था पायी जाती है।
|
इसमें ABC ABC परतीय व्यवस्था पाई जाती है।
|
|
3. इसमें अवयवी गोलों की संख्या छ: तथा उपसहसंयोजन संख्या (CN) = 12 व संकुलन क्षमता = 74% होती है।
|
इसमें अवयवी गोलों की संख्या चार तथा उपसहसंयोजन संख्या (CN) = 12 तथा संकुलन क्षमता 74% होती है।
|
| 4. उदाहरण : Zn , Mg आदि। | उदाहरण : Ag तथा cu आदि। |
FCC व CCP में चतुष्फलकीय एवं अष्टफलकीय रिक्तियों की संख्या व स्थान निर्धारण करना
2. अष्टफलकीय रिक्तियां : FCC एकक कोष्ठिका में अष्टफलकीय रिक्तियाँ केंद्र और किनारे पर पायी जाती है , FCC एकक कोष्ठिका के केन्द्र में एक पूर्ण अष्टफलकीय रिक्ति एवं प्रत्येक किनारे पर अष्टफलकीय रिक्ति का 1/4 भाग पाया जाता है , इस प्रकार एक FCC एकक कोष्ठिका में कुल अष्टफलकीय रिक्तियों की संख्या निम्न होगी।
अष्टफलकीय रिक्ति = केंद्र पर + किनारे पर
अष्टफलकीय रिक्ति = (1 x 1) + (1/4 x 12) = 1 + 3 = 4
FCC में अवयवी गोलों की संख्या = कोने पर + फलक पर
FCC में अवयवी गोलों की संख्या = (1/8 x 8) + (1/2 x 6) = 1 + 3 = 4 गोले
अत: FCC या CCP व HCP में अवयवी गोलों की संख्या के बराबर अष्टफलकीय रिक्तियां पाई जाती है तथा अवयवी गोलों की संख्या से दुगुनी चतुष्फलकीय रिक्तियाँ पायी जाती है।
किसी यौगिक में उपस्थित ऋण आयन FCC या CCP या HCP जालक का निर्माण करते है तथा धनायन चतुष्फलकीय या अष्टफलकीय रिक्तियों में भरे जाते है।
प्रश्न 1 : एक यौगिक x और y दो तत्वों से मिलकर बना है , y तत्व के परमाणु CCP संरचना बनाते है तथा x तत्व के परमाणु सभी अष्टफलकीय रिक्तियों को भरते है , इस यौगिक का सूत्र बताइये।
उत्तर : CCP संरचना में अष्टफलकीय रिक्ति व अवयवी गोलों के मध्य अनुपात 1:1 होता है , अत:
x : y
(सभी अष्टफलकीय रिक्तियों में उपस्थित धनायन) : (CCP संरचना में उपस्थित ऋण आयन)
1 : 1
यौगिक सूत्र = xy
प्रश्न 2 : एक यौगिक दो तत्वों M व N से मिलकर बना है , N तत्व के परमाणु HCP संरचना बनाते है तथा M तल के परमाणु चतुष्फलकीय रिक्तियों का 1/3 भाग भरते है इस यौगिक का सूत्र बताइए।
उत्तर : HCP संरचना में चतुष्फलकीय रिक्ति व अवयवी गोलों के मध्य अनुपात 2:1 होता है अत:
उत्तर : M : N
(चतुष्फलकीय रिक्ति के 1/3 भाग में उपस्थित धनायन) : (HCP संरचना में उपस्थित ऋण आयन)
2 x 1/3 : 1
2/3 x 3 : 1 x 3
2:3
अत: यौगिक का सूत्र M2N3 होगा।
प्रश्न 1 : एक यौगिक X तथा Y दो तत्वों से निर्मित है। Y तत्व के परमाणुओं (ऋणायन) से cpp बनता है तथा X तत्व के परमाणु (धनायन) सभी अष्टफलकीय रिक्तियों में भरे होते है। यौगिक का सूत्र क्या है।
चतुष्फलकीय तथा अष्टफलकीय रिक्तियों का स्थान निर्धारित करना (locating tetrahedral and octahedral voids)
हिंदी माध्यम नोट्स
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi sociology physics physical education maths english economics geography History
chemistry business studies biology accountancy political science
Class 12
Hindi physics physical education maths english economics
chemistry business studies biology accountancy Political science History sociology
English medium Notes
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi physics physical education maths entrepreneurship english economics
chemistry business studies biology accountancy
Class 12
Hindi physics physical education maths entrepreneurship english economics

