perkin reaction mechanism in hindi पर्किन अभिक्रिया का रासायनिक समीकरण उदाहरण सहित समझाइए
पर्किन अभिक्रिया का रासायनिक समीकरण उदाहरण सहित समझाइए perkin reaction mechanism in hindi ?
बेन्जॉइन संघनन (Benzoin Condensation)
यदि ऐरोमैटिक ऐल्डिहाइड को जलीय एथेनॉलिक पोटैशियम सायनाइड के साथ पश्चवाहित (reflux) किया जाता है तो बेन्जॉइन (Benzoin) बनता है। इस अभिक्रिया को बेंजोइन संघनन कहते हैं।
साधारणतया उपर्युक्त अभिक्रिया किसी क्षारक की उपस्थिति में न होकर सायनाइड आयन की उपस्थिति में होती है। इसका मुख्य कारण है-
(i) सायनाइड आयन नाभिक स्नेही अभिकर्मक के रूप में कार्बोनिल कार्बन पर आक्रमण करने में। सक्षम है।
(ii) कार्बन ऐनायन को अनुनाद के द्वारा स्थायित्व प्रदान करता है।
(iii) अन्तिम पद में CN® आयन कार्बन परमाणु से आसानी से बंध तोड़ सकता है।
जब दो भिन्न ऐल्डिहाइडों के मिश्रण को जलीय एथेनॉलिक पोटैशियम सायनाइड के साथ पश्चवाहित किया जाता है तो मिश्रित बेंजोइन और एकल बेंजोइन प्राप्त होते हैं ।
ऐलिफैटिक ऐल्डिहाइड यह अभिक्रिया नहीं देते हैं।
पर्किन अभिक्रिया (Perkins’s reaction)
जब बैन्जैल्डिहाइड (य़ा अन्य ऐरोमैटिक ऐल्डिहाइड) को किसी Q-हाइड्रोजन परमाणु वाले ऐलीफैटिक अम्ल के ऐनहाइड्राइड और उसके सोडियम लवण के साथ गर्म किया जाये तो B-ऐरिल ऐक्रिलिक अम्ल (a,p – असंतृप्त अम्ल) बनता है।
उदाहरणार्थ-
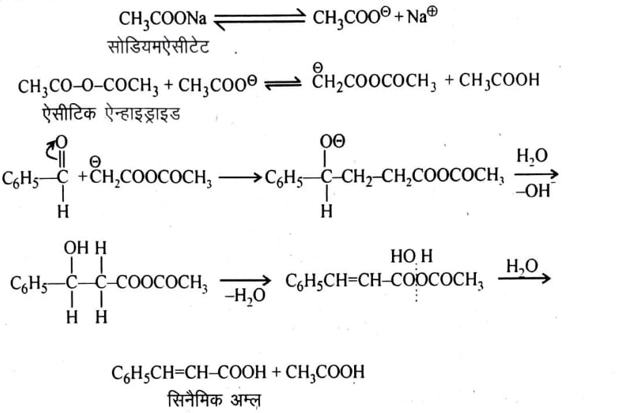
बेन्जैल्डिहाइड को ऐसीटिक एनहाइड्राइड और सोडियम ऐसीटेट के साथ गर्म करने पर सिनेमिक अम्ल प्राप्त होता है।
क्रियाविधि-
इसे बेजैल्डिहाइड की ऐसीटिक ऐन्हाइड्राइड एवं सोडियम ऐसीटेट के साथ अभिक्रिया से निम्न प्रकार समझा जा सकता है
ऐल्डोल संघनन (Aldol condensation)
ऐसे कार्बोनिल यौगिक (ऐल्केनैल अथवा ऐल्केनॉन) के दो अणु जिनमें – कार्बन परमाणु पर एक या अधिक हाइड्रोजन परमाणु उपस्थित होते हैं, दुर्बल तनु क्षार विलयन की उपस्थिति में स्वतः संघनित होकर ऐल्डोल बनाते हैं। यह अभिक्रिया ऐल्डोल संघनन कहलाती है। यह अभिक्रिया मेथेनैल द्वारा नहीं दी जाती है क्योंकि मेथेनैल में – हाइड्रोजन परमाणु उपस्थित नहीं होता है। मेथेनैल सान्द्र क्षार विलयन में कैनिजारो अभिक्रिया देता है (देखें मेथेनैल व्यक्तिगत सदस्य ) ।
एथेनैल के दो अणु आपस में दुर्बल क्षार K2CO3 अथवा Na2CO3 अथवा Ba(OH)2 विलयन की उपस्थिति में संयुक्त होकर ऐसीटैल्डोल (जो ऐल्डोल के नाम से जाना जाता है) बनाते हैं।
इसी प्रकार प्रोपेनॉन के दो अणु भी आपस में Ba(OH)2 की उपस्थिति में स्वतः संघनित होकर डाइ ऐसीटोन ऐल्कोहॉल बनाते हैं।
ऐल्डोल संघनन केवल ऐल्केनैल के दो अणुओं अथवा ऐल्केनॉन के दो अणुओं के मध्य ही नहीं होता वरन् यह एक अणु ऐल्केनैल और एक अणु ऐल्केनोन के मध्य भी संभव है और इनके संघनन से मिश्रित ऐल्डोल बनते हैं। जैसे ऐथेनैल और प्रोपेनॉन KCN की उपस्थिति में संघनित होकर 4-हाइड्रॉक्सी-2- पेन्टेनॉन बनाते हैं।
इस प्रकार ऐल्केनैल और ऐल्केनॉन के ऐल्डोल संघनन से प्राप्त उत्पादों में कार्बोनिल समूह की B-स्थिति पर एक हाइड्रॉक्सी समूह होता है और ऐसे यौगिक खनिज अम्लों की अल्प मात्रा में अथवा गर्म करने पर अथवा NaHSO4 के साथ गर्म करने पर जल का एक अणु त्याग देते हैं और a, p- असंतृप्त ऐल्केनैल तथा ऐल्केनॉन बनाते हैं।
क्रियाविधि (Mechanism ) – ऐल्केनैल अथवा ऐल्केनॉन का एक अणु तनु क्षार विलयन के साथ अभिकृत होकर a-कार्बन परमाणु से एक प्रोटॉन त्यागकर ऐनायन बनता है जो अनुनाद द्वारा स्थायी होता है, इसमें ऋणावेश कार्बन तथा ऑक्सीजन दोनों परमाणुओं पर अस्थानीकृत रहता है। ऐसे ऐनायन ईनोलेट (enolate) कहलाते हैं। यह माना जाता है कि ऐसे कार्बोनिल यौगिक जिनमें अनुनाद द्वारा स्थायी ऐनायन प्राप्त हो सकते हैं उनमें सक्रिय मेथिलीन समूह उपस्थित होता है। ये ऐनायन कार्बन-नाभिक स्नेही की भाँति ऐल्केनैल अथवा ऐल्केनोन के दूसरे अणु से योगात्मक अभिक्रिया करके योगोत्पाद (ऐल्डोल) दे देते हैं। इसे एथेनैल का उदाहरण लेकर निम्न प्रकार समझाया जा सकता है-
बेरियम हाइड्रॉक्साइड की उपस्थिति में ऐसीटोन संघनित होकर डाइऐसीटोन ऐल्कोहॉल देता है ।
शुष्क HCI की उपस्थिति में ऐसीटोन के दो अणु संघनित होकर मेसिटिल ऑक्साइड बनाते हैं जो पुनः ऐसीटोन के एक अणु के साथ संघनन पर फोरोन देता है।
सल्फ्यूरिक अम्ल की उपस्थिति में ऐसीटोन के तीन अणु संघनित होकर एक चक्रीय यौगिक मेसिटिलीन बनाते हैं।
फार्मेल्डिहाइड का संघनन (Condensation of formadehyde ) :- फोर्मेल्डिहाइड में यद्यपि, हाइड्रोजन परमाणु नहीं होता है तथापि यह ऐल्डोल संघनन दर्शाता है। बेरियम हाड्रॉक्साइड के तनु विलयन में फॉर्मेल्डिहाइड संघनित होकर फार्मेस देता है।
नोवेनेजैल संघनन (Knoevenagel Condensation)
एक ऐल्डिहाइड या कीटोन की कार्बनिक क्षार की उपस्थिति में अभिक्रियाशील मेथिलीन समूह युक्त यौगिक के साथ अभिक्रिया नोवेनेजैल संघनन कहलाती है।
उपर्युक्त अभिक्रिया में ऐल्डिहाइड एवं एथिल मैलोनेट की तुल्यांकी मात्रायें लेते हैं और पिरिडीन क्षार के रूप प्रयुक्त करते है। यदि एथिलमैलोनेट अधिकता में लें तो पिपरैडिन की उपस्थिति में उपर्युक्त अभिक्रिया का उत्पाद एथिलमैलोनेट से पुनः अभिक्रिया कर लेता है। इस अभिक्रिया को माइकेल संघनन कहते हैं।
अतः नोवेनेजैल संघनन से तात्पर्य केवल उस संघनन से है जिसमें असंतृप्त यौगिक प्राप्त होता है। ये असंतृप्त यौगिक जल अपघटन और फिर गर्म करने पर a, B – असंतृप्त अम्ल बनाते हैं।
एथिल मैलोनेट केवल ऐल्डिहाइडों के साथ ही संघनित होता है। एथिलऐसीटोएसीटेट ऐल्डिहाइड एवं कीटोन दोनों के साथ संघनित जाता है, उदाहरणार्थ-
कीटोन की एथिल सायनोएसीटेट के साथ ऐमीनो अम्ल क्षार की उपस्थिति में संघनित अभिक्रिया हो जाती है। प्राप्त उत्पाद शीघ्रता से कार्बोक्सिलिक अम्ल में जल अपघटित हो जाता है।
क्रियाविधि – इसे एक ऐल्डिहाइड की डाइएथिलमैलोनेट साथ पिरिडीन (तृतीयक क्षार) की उपस्थिति में संघनन अभिक्रिया से निम्न प्रकार समझा जा सकता है-
नोवेनैजेल अभिक्रिया उत्क्रमणीय होती है जिससे उत्पाद की कम लब्धि प्राप्त होती है। इस हेतु कोप (Cope) ने सुझाया कि यदि अभिक्रिया बैंजीन माध्यम में कराई जाए तथा बैंजीन एवं जल के मिश्रण को स्थिरक्वाथी मिश्रण (Azeotropic mixiure) के रूप में निकाला जाए तो साम्य दांई ओर विस्थापित हो जाता है तथा उत्पाद की लब्धि अधिक प्राप्त होती है अतः यह अभिक्रिया कोप नोवेनैजेल (Cope Knoevenagel’s reaction) कहलाती है।
कार्बोनिल यौगिकों का अमोनिया एवं अमोनिया व्युत्पन्नों के साथ संघनन (Condensation of Carbonyl Compounds with Ammonia and Ammonia Derivatives)
कार्बोनिल यौगिकों की अमोनिया व्युत्पन्नों के साथ अभिक्रिया
अमोनिया व्युत्पन्न नाइट्रोजन नाभिक स्नेही यौगिक हैं। इनमें N – परमाणु पर एकाकी इलेक्ट्रॉन युग्म उपस्थित होने के कारण यह नाभिक स्नेही केंद्र होता है। नाइट्रोजन नाभिक स्नेही कार्बोनिल समूह पर कार्बन नाभिक स्नेही की अपेक्षा कम प्रभावी रूप से योग करते हैं। नाइट्रोजन नाभिक स्नेही साधारणतः अमोनिया व्युत्पन्न (H2NZ) होते है, जहाँ Z निम्नलिखित समूह हो सकता है-
कार्बोनिल समूह पर अमोनिया व्युत्पन्नों की अभिक्रिया को निम्न प्रकार प्रदर्शित कर सकते हैं- >C=O+H2N-Z→>C=N-Z+H2O
क्रिया – विधि – HN – Z नाभिक स्नेही अभिकर्मकों से अभिक्रिया की क्रियाविधि को निम्नलिखित पदों द्वारा प्रदर्शित कर सकते हैं।
(अ) नाभिकस्नेही द्वारा कार्बोनिल कार्बन पर आक्रमण-
(ब) नाइट्रोजन परमाणु से ऑक्सीजन परमाणु पर प्रोटोन (ii) का स्थानान्तरण-
(स) जल के अणु का अन्तःअणुक (Intermolecular) विलोपन-
अतः सम्पूर्ण अभिक्रिया को सरल रूप में निम्नलिखित प्रकार प्रदर्शित कर सकते हैं-
इस सरल समीकरण को देखकर लगता है कि यह अभिक्रिया संघनन अभिक्रिया है परन्तु इसमें पहले नाभिक स्नेही का योग होता है और बाद में योगोत्पाद से जल से एक अणु का विलोपन होता है।
(i) हाइड्रॉक्सिल ऐमीन से योग- ऐल्केनैल तथा ऐल्केनॉन हाइड्रॉक्सिल ऐमीन से अभिक्रिया करके संगत ऑक्सिम बनाते हैं-
(ii) हाइड्रैजीन से योग- ऐल्केनैल तथा ऐल्केनॉन हाइड्रैजीन से अभिक्रिया करके संगत हाइड्रैजोन बनाते हैं।
(iii) फेनिल हाइड्रैजीन से योग- ऐल्केनैल तथा ऐल्केनोन फेनिल हाइड्रैजीन से अभिक्रिया करके संगत फेनिल हाइड्रेजोन बनाते हैं।
(iv) 2,4-डाइनाइट्रो फेनिल हाइड्रैजीन से योग- 2,4- डाइनाइट्रो फेनिल हाइड्रैजीन से अभिक्रिया करके ये संगत 2,4-डाइनाइट्रो फेनिल हाइड्रेजोन बनाते हैं। ये पीले रंग के क्रिस्टलीय ठोस पदार्थ होते हैं। यह अभिक्रिया कार्बोनिल समूह के परीक्षण में काम आती है।
(v) सेमीकार्बेजाइड से योग– ऐल्केनैल तथा ऐल्केनॉन सेमीकार्बेजाइड से अभिक्रिया करके संगत सेमीकार्बेजोन बनाते हैं।
(vi) ऐमीन से योग- ऐल्केनैल तथा ऐल्केनॉन दोनों ही प्राथमिक ऐमीन के साथ अभिक्रिया कर शिफक्षार (इमीन) बनाते हैं। ऐल्केनॉन के साथ अभिक्रिया कठिनाई से होती है, परन्तु उत्प्रेरक जैसे शुष्क जिंक क्लोराइड आदि की उपस्थिति में सुगमता से सम्भव है।
हिंदी माध्यम नोट्स
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi sociology physics physical education maths english economics geography History
chemistry business studies biology accountancy political science
Class 12
Hindi physics physical education maths english economics
chemistry business studies biology accountancy Political science History sociology
English medium Notes
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi physics physical education maths entrepreneurship english economics
chemistry business studies biology accountancy
Class 12
Hindi physics physical education maths entrepreneurship english economics