organic compounds of nitrogen in hindi नाइट्रोजन के कार्बनिक यौगिक युक्त notes
नाइट्रोजन के कार्बनिक यौगिक युक्त notes organic compounds of nitrogen in hindi ?
नाइट्रोजन के कार्बनिक यौगिक (Organic Compounds of Nitrogen)
नाइट्रोऐल्केन (Nitroalkane)
ऐल्केन में से H-परमाणु को नाइट्रो समूह के द्वारा प्रतिस्थापित करने पर नाइट्रोऐल्केन बनते हैं। नाइट्रोसमूह प्राथमिक, द्वितीयक एवं तृतीयक C-परमाणु पर उपस्थित होने पर इन्हें क्रमशः प्राथमिक. द्वितीयक एवं तृतीयक नाइट्रोऐल्केन कहते हैं।
8.1.1 विरचन की विधियाँ
(1) ऐल्किल हैलाइड को जलीय एथेनॉलिक सिल्वर नाइट्राइट विलयन के साथ गर्म करने पर-
RX + Ag—O—N=0 – R – NO2 + R – O-N= O + AgX
यह विधि केवल प्राथमिक नाइट्रोऐल्केन बनाने के लिये प्रयुक्त होती है। द्वितीयक एवं तृतीयक हैलाइडों के साथ लब्धि केवल 5 से 15% होती है।
कार्नबल्म (Kornblun, 1956) के अनुसार ऐल्किल हैलाइड सोडियम नाइट्राइट के साथ अभिक्रिया करके 55-62% तक की लब्धि में नाइट्रोएल्केन बनाते हैं। 25-33% ऐल्किल नाइट्राइट भी बनता है । डाइमेथिल फॉर्मेमाइड (DMF) विलायक लेने पर और यूरिया मिलाने पर नाइट्रोऐल्केन की अधिक लब्धि प्राप्त होती है।
RX + NaNO2→→ R – NO2 + R – O – N = O + NaX
(55-62%) (25-33%)
स्माइले एवं फ्रीडेमेन (1960) के अनुसार यदि विलायक डाइमेथिलसल्फॉक्साइड (DMSO) लें तो यूरिया डालने की आवश्यकता नहीं होती है।
नाइट्रोमेथेन को जलीय सोडियम नाइट्राइट को क्लोरोऐसीटिक अम्ल के साथ उबालकर बनाया जा सकता है।
CICH2COOH + NaNO2 >>>> CH3NO2 + CO2
(35-38%)
(2) नाइट्रोयौगिकों का औद्योगिक संश्लेषण प्रत्यक्ष नाइट्रीकरण विधि के द्वारा करते हैं। नाइट्रीकरण दो प्रावस्थाओं में करते हैं-
(i) द्रव-प्रावस्था नाइट्रीकरण हाइड्रोकार्बन को सांद्र HNO3 के साथ 140°C पर उच्च दाब पर गर्म करते हैं। इस प्रकार का नाइट्रीकरण धीमी गति से होता है और पॉलिनाइट्रो यौगिक बनते हैं।
(ii) वाष्प-प्रावस्था नाइट्रीकरण- इसमें हाइड्रोकार्बन को नाइट्रिक अम्ल या नाइट्रोजन के ऑक्साइड के साथ 350-475°C पर गर्म करते हैं। प्रत्येक हाइड्रोकार्बन के लिये यह ताप भिन्न भिन्न होता है।
(3) तृतीयक कार्बोनेमीन का पोटैशियम परमैंगनेट के साथ ऑक्सीकरण करने पर तृतीयक नाइट्रोयौगिक प्राप्त होते हैं। (कॉर्नबल्स, 1956)
8.1.2 नाइट्रोऐल्केन की रासायनिक अभिक्रियाएँ (Chemical Reactions of Nitroalkanes )
(1) अपचयन- (i) नाइट्रोऐल्केन लीथियम ऐलुमिनियम हाइड्राइड या धातु-अम्ल या उत्प्रेरित हाइड्रजनीकरण के द्वारा अपचयन पर प्राथमिक ऐमीन में बदल जाते हैं।
(ii) नाइट्रोऐल्केन का अपचयन धातु के साथ उदासीन माध्यम में करने पर N – ऐल्किलहाइड्रॉक्सिलऐमीन प्राप्त होते हैं।
(ii) स्टैनस क्लोराइड एवं हाइड्रोक्लोरिक अम्ल से अपचयन पर नाइट्रोयोगिकों का N – ऐल्किल हाइड्रॉक्सिल ऐमीन तथा ऑक्सिम के मिश्रण में परिवर्तन हो जाता है।
(2) जलअपघटन- (i) प्राथमिक नाइट्रोएल्केनों को 85% H2SO4 या HCI के साथ उबालने पर इनका जलअपघटन होकर कार्बोक्सिलिक अम्ल तथा हाइड्रॉक्सिलऐमीन बनते हैं।
यह अभिक्रिया हाइड्रॉक्सिल ऐमीन बनाने में प्रयुक्त होती है।
(ii) द्वितीयक नाइट्रोऐल्केन को HCI के साथ उबालने पर ये जलअपघटित होकर कीटोन एवं नाइट्रस ऑक्साइड बनाते हैं।
तृतीयक नाइट्रोयौगिकों का हाइड्रोक्लोरिक अम्ल से जलअपघटन नहीं हो पाता है।
(3) नाइट्रोऐल्केन में चलावयवता- प्राथमिक एवं द्वितीयक नाइट्रोऐल्केन जिनमें Q-H परमाणु उपस्थित होता है, चलावयवता प्रदर्शित करते हैं।
नाइट्रो अवस्था (I) को स्यूडो-अम्ल (Pseudo acid) अवस्था तथा आइसोनाइट्रो अवस्था (II) को ऐसिअवस्था (Aci form) अथवा नाइट्रोलिक अम्ल कहते हैं।
नाइट्रो यौगिक जलीय NaOH में घुलकर Na-लवण बनाते हैं।
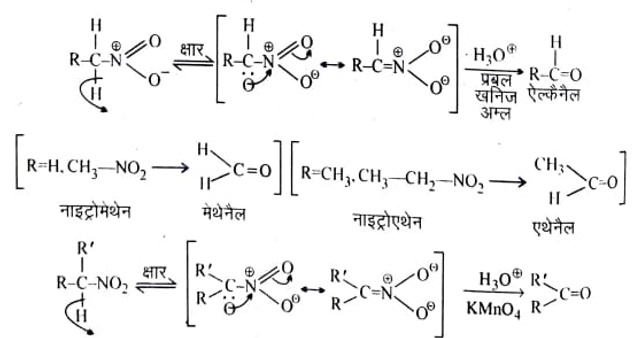
प्राथमिक नाइट्रोऐल्केन एवं द्वितीयक नाइट्रोऐल्केन के संगत नाइट्रोलिक अम्ल के Na – लवण को 50% सल्फ्यूरिक अम्ल से अम्लीकृत करने पर क्रमशः ऐल्डिहाइड एवं कीटोन प्राप्त होते हैं। इस अभिक्रिया को नेफ कार्बोनिल संश्लेषण कहते हैं
नाइट्रोलिक अम्ल के सोडियम लवण का SnCI 2 / HCI से अपचयन करने पर ऐल्डॉक्सिम तथा कीटो ऑक्सिम बनते हैं ।
(4) हैलोजनीकरण- प्राथमिक एवं द्वितीयक नाइट्रोएल्केन की क्षारकीय माध्यम हैलोजन के साथ अभिक्रिया पर a-हैलो नाइट्रोऐल्केन प्राप्त होते हैं। Q- स्थिति पर जितने भी H – परमाणु उपस्थित होते है उन सभी का प्रतिस्थापन हो जाता है।
नाइट्रोमेथेन की क्लोरीन के साथ NaOH की उपस्थिति में अभिक्रिया से क्लोरोपिक्रिन बनता है।
CH3NO2 + 3Cl2 + 3NaOHC CI3CNO2 + 3NaCl + 3H2O
(5) नाइट्रस अम्ल के साथ प्राथमिक नाइट्रोऐल्केन की नाइट्रस अम्ल के साथ अभिक्रिया से नाइट्रोलिक अम्ल बनते हैं जो NaOH विलयन में घुलकर लाल रंग देते हैं।
द्वितीयक नाइट्रोऐल्केन नाइट्रस अम्ल के साथ अभिक्रिया करके स्यूडोनाइट्रोल बनाते हैं। ये NaOH में घुलकर नीला रंग देते हैं।
ये अभिक्रियाऐं p. s एवं 1- ऐल्कोहॉल के विभेद में प्रयुक्त होती हैं (विक्टर मेयर परीक्षण) ।
(6) प्राथमिक एवं द्वितीयक नाइट्रोऐल्केन में सक्रिय H परमाणु उपस्थित होने के कारण ये ऐल्डिहाइड के साथ संघनित अभिक्रिया कर लेते हैं। उदाहरणार्थ- नाइट्रोमेथेन, बेंजेल्डिहाइड के साथ ऐल्कोहॉलिक KOH की उपस्थिति में अभिक्रिया करके 10- नाइट्रोस्टाईरीन बनाता है।
नाइट्रोऐल्केन a,B- असंतृप्त कीटोन के साथ भी अभिक्रिया करके योगात्मक यौगिक बना लेते है।
यह माइकेल संघनन का उदाहरण है।
प्राथमिक एवं द्वितीयक नाइट्रोऐल्केन मैनिक अभिक्रिया भी देते है। अध्याय-5 में मैनिक अभिक्रिया
8.2 नाइट्रोऐरीन (Nitroarenes)
ऐरोमैटिक हाइड्रोकार्बन में उपस्थित एक या अधिक हाइड्रोजन परमाणुओं का नाइट्रो समूह
द्वारा प्रतिस्थापन करने पर ऐरोमैटिक नाइट्रो यौगिक प्राप्त होते हैं। यह प्रतिस्थापन अभिक्रिया नाइट्रीकरण (Nitration) कहलाती है।
(i) वे यौगिक जिनमें नाइट्रो समूह बेंजीन वलय से जुड़ता है, इसके कुछ उदाहरण निम्न प्रकार हैं –
(ii) वे जिनमें नाइट्रो समूह बेंजीन वलय में उपस्थित किसी श्रृंखला में जुड़ता है, जैसे फेनिल नाइट्रो मेथेन ।
8.2.1 नाइट्रोऐरीन बनाने की विधियाँ
2-फेनिल नाइट्रोएथेन
ऐरोमैटिक नाइट्रो यौगिक ऐरोमैटिक हाइड्रोकार्बन के सीधे नाइट्रीकरण से प्राप्त किए जाते हैं। नाइट्रीकरण के लिए साधारणतः निम्नलिखित अभिकर्मकों का प्रयोग करते हैं।
(1) सांद्र नाइट्रिक अम्ल
(2) सधूम नाइट्रिक अम्ल ( नाइट्रिक अम्ल + नाइट्रोजन डाइऑक्साइड)
(3) नाइट्रीकरण मिश्रण – सान्द्र नाइट्रिक अम्ल और सांद्र सल्फ्यूरिक अम्ल का मिश्रण (सल्फ्यूरिक अम्ल के स्थान पर ग्लैशल ऐसीटिक अम्ल अथवा बोरोन ट्राइफ्लुओराइड का उपयोग भी करते हैं।) (4) ऐसीटिल नाइट्रेट
5. तनु नाइट्रिक अम्ल :-
कुछ सक्रिय यौगिक जैसे फीनॉल का नाइट्रीकरण तनु HNO3 से किया जा सकता है। इस अभिक्रिया में NO2 के स्थान पर NO इलेक्ट्रॉनिक स्नेही के रूप में कार्य करता है इसके परिणामस्वरूप नाइट्रोसोबैंजीन प्राप्त होता है जो HNO3 के द्वारा ऑक्सीकृत होकर नाइट्रोबैंजीन बनाता है। क्रियाविधि निम्न लिखित प्रकार है।
बेंजीन वलय में जुड़ने वाले नाइट्रो समूहों की संख्या तथा सुगमता निम्नलिखित कारकों पर निर्भर करती है-
(1) नाइट्रीकृत होने वाले पदार्थ का स्वभाव (Nature of the compound which is to be nitrated) – यदि नाइट्रीकृत होने वाले यौगिक की बेंजीन वलय पर सक्रियणकारी समूह जैसे – OH- NH2;- OR (ऑर्थो एवं पैरा निदेशक) उपस्थित हों तो नाइट्रीकरण सुगमता से हो जाता है। असक्रियणकारी, मेटा निदेशी समूह जैसे –NO2, –CN, CHO, COOH आदि उपस्थित होने पर नाइट्रीकरण कठिनाई से होता है। उदाहरणार्थ-
(2) नाइट्रीकारक का स्वभाव (Nature of the nitrating agent ) ऐसे नाट्रीकारक जिनसे नाइट्रोनियम आयन सुगमता से बन जाता है, अच्छे नाइट्रीकारक अभिकर्मक होते हैं। सान्द्र नाइट्रिक अम्ल तथा सांद्र सल्फ्यूरिक अम्ल के मिश्रण के स्पेक्ट्रमी अध्ययन से मालूम हुआ कि इसमें नाइट्रोनियम आयन NO2, उपस्थित होता है। कुछ स्थायी यौगिकों जैसे नाइट्रोनियम क्लोरेट NO2CID4 नाइट्रोनियमफ्लुओरोबोरेट, NO2BF4 एवं नाइट्रोनियमफ्लुओरो फॉस्फेट NO2PF6 से नाइट्रीकरण सुगमता से हो जाता है। इससे प्रमाण मिलता है कि इलेक्ट्रॉनस्नेही ऐरोमैटिक नाइट्रीकरण में नाइट्रोनियम आयन NO2ही इलेक्ट्रॉनरनेही के रूप में प्रयुक्त होता है।
(3) अभिक्रिया का ताप (Reaction temperature) – कम ताप पर मोनोनाइट्रो व्युत्पन्न और उच्च ताप पर डाइ अथवा ट्राइनाइट्रो व्युत्पन्न प्राप्त होते है।
(4) त्रिविम कारक (Steric factors) – अन्य परिस्थितियों के समान होने पर भी नाइट्रीकृत होने वाले यौगिकों में बेंजीन वलय पर बड़े आकार वाले समूह (Bulky groups ) उपस्थित होने पर नाइट्रीकरण प्रभावित होता है, उदाहरणार्थ –
नोट- नाइट्रीकरण की क्रियाविधि आप B.Sc. Pt में पढ़ चुके हैं।
प्रयोगशाला में बेंजीन पर सान्द्र नाइट्रिक अम्ल और सांद्र सल्फ्यूरिक अम्ल के मिश्रण ( नाइट्रीकरण मिश्रण) की अभिक्रिया द्वारा जल ऊष्मक पर 50-60°C ताप पर पश्चवाहित (Reflex) करने से प्राप्त होता है।
नाइट्रोऐरीन बनाने की अन्य विधियाँ
(i) डाइऐजोनियम लवणों की प्रतिस्थापन अभिक्रिया द्वारा:- p-नाइट्रोऐरीन का डाइऐजोटीकरण NaNO2 तथा HBF4 से कराते हैं। प्राप्त यौगिक की अभिक्रिया NaNO2 तथा HCI के साथ कराने पर P-डाइनाट्रोबैंजीन प्राप्त हो जाती है।
(ii) ऐमीनो यौगिकों के सीधे ऑक्सीकरण द्वारा :-p- नाइट्रोऐनिलीन के सीधे ऑक्सीकरण द्वारा p डाइनाइट्रोबेंजीन बनती है। ऑक्सीकारक के रूप में परसल्फ्यूरिक अम्ल, परॉक्सीट्राइफ्लुओरोऐसिटिक अम्ल का उपयोग करते हैं।
8.2.2 नाइट्रोऐरीन में नाभिक स्नेही प्रतिस्थापन एवं उसकी क्रियाविधि नाइट्रोऐरीन में नाभिक स्नेही प्रतिस्थापन अभिक्रियाऐं कठिनाई से होती है। इसके निम्नलिखित कारण हैं –
(i) ऐरोमैटिक वलय का ग-इलेक्ट्रॉन अभ्र नाभिक स्नेही अभिकर्मक को प्रतिकर्षित करता है। (ii) वलय के C-परमाणु और नाइट्रो समूह के N- परमाणु के मध्य बंध ऐलिफैटिक नाइट्रो यौगिकों की अपेक्षा अधिक मजबूत होता है क्योंकि बंध बनाने में वलय का C- परमाणु sp2 संकरित कक्षक का उपयोग करता है जबकि ऐलिफैटिक यौगिकों में sp3 संकरित कक्षक प्रयुक्त करता है।
तीव्र परिस्थितियों में ये ऐरीन व्युत्पन्न एक इलेक्ट्रॉन आकर्षी समूह जैसे – NO2. CN, COOH आदि उपस्थित होने पर SN2 ऐरोमैटिक अभिक्रियाऐं देते हैं। इनमें हाइड्राइड आयन (H) का प्रतिस्थापन होता है।
उदाहरणार्थ – नाइट्रोबेंजीन को ठोस KOH के साथ वायु की उपस्थिति में संगलित करने पर 0- नाइट्रोफीनोल (मुख्य उत्पाद) और p- नाइट्रोफीनोल (थोड़ी सी मात्रा ) में बनता है। अभिक्रिया की क्रियाविधि निम्न प्रकार है –
यदि NO2 समूह के o अथवा p-स्थिति पर इलेक्ट्रॉन आकर्षी समूह उपस्थित हो तो NO, समूह को अन्य नाभिक स्नेही द्वारा सुगमता से प्रतिस्थापन किया जा सकता है। उदाहरणार्थ –
o-एवं p-डाइनाइट्रोबेंजीन में एक नाइट्रो समूह का -1 तथा – M प्रभाव वलय के उस C- परमाणु पर इलेक्ट्रॉन घनत्व कम कर देता है जिस पर दूसरा – NO2 समूह उपस्थित होता है। इस प्रकार इस C- परमाणु पर नाभिकस्नेही आक्रमण सुगमता से हो जाता है। उदाहरणार्थ – p-डाइनाइट्रोबेंजीन की जलीय NaOH के साथ अभिक्रिया की क्रियाविधि निम्न प्रकार है-
8.2.3 नाइट्रोऐरीन का विभिन्न माध्यमों में अपचयन –
नाइट्रोऐरीन के विभिन्न माध्यमों में अपचयन का वर्णन नाइट्रोबेंजीन का उदाहरण लेकर निम्न प्रकार कर सकते हैं। नाइट्रोबेंजीन का शीघ्रता से अपचयन हो जाता है। अपचयन के फलस्वरूप बनने वाला उत्पाद अपचायक की प्रकृति और अभिक्रिया के माध्यम पर निर्भर करता है। इसका अपचयन निम्नलिखित क्रम में होता है।
साधारणतया नाइट्रोबेंजीन के अम्लीय माध्यम में अपचयन पर ऐनिलीन और उदासीन माध्यम में अपचयन पर फेनिल हाइड्रॉक्सिल ऐमीन प्राप्त होता है। क्षारीय माध्यम में यह हाइड्रेजोबेंजीन, ऐजोबेंजीन और ऐजोक्सीबेंजीन में अपचयित हो जाता है। उत्पाद लिए गए अपचायक पर निर्भर करता है । नाइट्रोबेंजीन का विद्युत अपघटनी अपचयन करने पर p-ऐमीनों फीनोल मुख्य उत्पाद के रूप में प्राप्त होता है। विद्युत अपघटनी अपचयन सांद्र सल्फ्यूरिक अम्ल की उपस्थिति में कराया जाता है। विभिन्न माध्यमों में विभिन्न अपचायकों की अभिक्रिया नीचे दी गई है
(1) अम्लीय माध्यम में अपचयन नाइट्रोबेंजीन का अपचयन Sn/ सांन्द्र HCI या Fe/ सांद्र HCI या SnCl2/ सान्द्र HCI या TiCl3 / सान्द्र HCI से करने पर नाइट्रो समूह ऐमीनो समूह में अपचयित हो जाता है।
(ii) उदासीन माध्यम में अपचयन उदासीन माध्यम में Zn एवं NH4CI से अपचयन करने पर फेनिल हाइड्रॉक्सिल ऐमीन बनता है।
(iii) क्षारकीय माध्यम में अपचयन नाइट्रोबेंजीन के क्षारकीय माध्यम में अपचयन के क्रम को निम्न प्रकार प्रदर्शित कर सकते हैं।
क्षारकीय माध्यम में नाइट्रोबेंजीन का अपचयन विभिन्न अपचायकों से करने पर भिन्न-भिन्न उत्पाद प्राप्त होते हैं-
(a) CH3OH/NaOH या ग्लूकोस / NaOH से अपचयन पर ऐजॉक्सीबेंजीन प्राप्त होती है।
(b) SnCI2+ NaOH से अपचयन पर ऐजोबेंजीन बनती है।
(c) Zn + NaOH से अपचयन पर हाइड्रैजोबेंजीन प्राप्त होती है।
(iv) विद्युत अपघटन अपचयन (Electrolytic reduction) – नाइट्रोबेंजीन का सांद्र H2SO4 की उपस्थिति में विद्युत अपघटनी अपचयन करने पर p-ऐमीनो फीनोल बनता है।
(v) उत्प्रेरित अपचयन नाइट्रोबेंजीन का Ni या Pt उत्प्रेरक की उपस्थिति में हाइड्रोजन से अपचयन करने पर ऐनिलीन बनती है।
नाइट्रोबेंजीन की इलेक्ट्रॉनस्नेही प्रतिस्थापन अभिक्रियाएँ निम्नलिखित है ।
(i) नाइट्रीकरण :- नाइट्रोबैंजीन की अभिक्रिया 100°C पर सान्द्र HNO3 से कराने पर m- डाइनाइट्रोबैंजीन प्राप्त होती है।
(ii) हैलोजनीकरण :- हैलोजनीकरण की उपस्थिति में नाइट्रोबैंजीन का हैलोजनीकरण करवाने पर m – क्लोरोनाइट्रोबैंजीन बनता है।
(iii) सल्फोनीकरण :- सधूम H2SO4 के साथ नाइट्रोबैंजीन, m – नाइट्रोसल्फोनिक अम्ल देता है।
नाइट्रोबेंजीन फ्रीडेल क्राफ्ट अभिक्रियाऐं नही देता है।