Carboxylic Acids in hindi notes definition कार्बोक्सिलिक अम्ल नोट्स कक्षा बीएससी उदाहरण परिभाषा
कार्बोक्सिलिक अम्ल नोट्स कक्षा बीएससी उदाहरण परिभाषा Carboxylic Acids in hindi notes definition ?
कार्बोक्सिलिक अम्ल (Carboxylic Acids)
परिचय (Introduction)
प्राकृतिक वसा में पामिटिक अम्ल (C15H31 – COOH) और स्टिऐरिक अम्ल C17H35 — COOH, वसीय अम्ल प्राप्त होते हैं जो ऐल्कनोइक अम्ल सजातीय श्रेणी के उच्च सदस्य हैं अतः इस श्रेणी के सजातीय यौगिकों को वसीय अम्ल कहते हैं। इस श्रेणी का सामान्य सूत्र CH2O2 होता है और इसमें – COOH समूह होने के कारण इसको निम्न प्रकार लिखा जा सकता है-
CnH(2n+1)COOH या _ R – COOH (जहाँ R= H या ऐल्किल समूह) ।
|-COOH समूह को सर्वप्रथम बायर नामक वैज्ञानिक ने कार्बोक्सिलिक समूह नाम दिया था। उपर्युक्त सामान्य सूत्र से प्रदर्शित कार्बनिक अम्ल संतृप्त यौगिक होते हैं और इनमें एक ही – COOH समूह होता है। इसलिए इन्हें संतृप्त मोनो कार्बोक्सिलिक अम्ल भी कहते हैं। कार्बोक्सिलिक समूह की संरचना साधारणतः द्वारा लिखी जाती है।
नामकरण एवं समावयवता (Nomenclature and Isomerism)
वसीय अम्ल साधारणतः उनके रूढ़ नामों से जाने जाते हैं। यह नाम उनके प्राप्ति के मूल स्रोत के आधार पर दिया जाता है । जैसे H-COOH, फॉर्मिक अम्ल को यह नाम इसलिए दिया गया क्योंकि सर्वप्रथम इसको चींटियों के आसवन से प्राप्त किया गया था, जिन्हें लेटिन भाषा में फॉर्मिका (Formica) कहते हैं। इसी प्रकार CH3COOH, ऐसीटिक अम्ल सिरके (vinegar) का मुख्य अवयव है जिसका लेटिन नाम ऐसीटम (acetum) है।
नामकरण की दूसरी पद्धति में फार्मिक अम्ल के अतिरिक्त अन्य सभी अम्लों को ऐसीटिक अम्ल का | व्युत्पन्न माना जाता है।
उपर्युक्त इन दोनों पद्धतियों में श्रृंखला में उपस्थित अन्य क्रियात्मक समूहों (प्रतिस्थापियों) की स्थिति को ग्रीक अक्षरों (Greek letters) a, B, Y और 8 आदि से दर्शाते हैं। कार्बोक्सिलिक समूह से बन्धित कार्बन को a, उनके बाद वाले को 3-आदि कहते हैं। उदाहणार्थ-
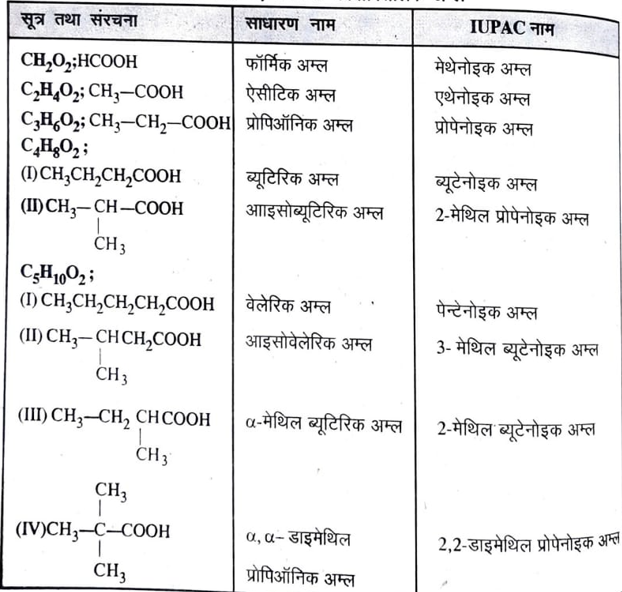
नामकरण की आई. यू. पी. ए. सी पद्धति में इन्हें ऐल्केनोइक अम्ल कहते हैं जिसे संगत ऐल्केन ( alkane) से अंग्रेजी के अक्षर ‘ई’ (e) को हटाकर अनुलग्न ओइक अम्ल (oic acid) लगाकर प्राप्त करते हैं । जैसे- H-COOH मेथेनोइक अम्ल, CH3 – COOH एथेनोइक अम्ल आदि । R – C – समूह को ऐसिल समूह कहते हैं और इसका नाम संगत ऐल्केनोइक अम्ल (alkanoic acid) से इक अम्ल (ic acid) हटाकर प्राप्त किया जाता है। जैसे मेथेनोइक अम्ल से मेथेनोयल और एथेनोइक अम्ल से एथेनोयल आदि। पांच कार्बन तक के अम्लों के मोनो कार्बोक्सिलिक अम्लों के साधारण तथा IUPAC नाम सारणी 6.1 में दिये गये हैं ।
सारणी 6.1 ऐलिफैटिक कार्बोक्सिलिक अम्ल
प्रतिस्थापित कार्बोक्सिलिक अम्ल – प्रतिस्थापित कार्बोक्सिलिक अम्ल में उस दीर्घतम श्रृंखला का चयन करते हैं जिसमें सभी प्रतिस्थापी एवं – COOH समूह उपस्थित हों। -COOH समूह के C परमाणु को संख्या – 1 देते हैं। अन्य प्रतिस्थापियों की शृंखला पर स्थिति दर्शाते हुए उनके नामों को अंग्रेजी वर्णमाला के क्रम में ऐल्कनोइक अम्ल के नाम से पूर्व लिख देते हैं। उदाहरणार्थ-
चक्रीय कार्बोक्सिलिक अम्लों के नामकरण-
. वे कार्बोक्सिलिक अम्ल जिनमें – COOH समूह वलय निकाय (ring system) से जुड़ा होता है, का IUPAC नामकरण वलय के नाम के साथ कार्बोक्सिलिक अम्ल अनुलग्नित करके दिया जाता है। उदाहरणार्थ—
यदि चक्रीय वलय में प्रतिस्थापी उपस्थित हों तो – COOH समूह को संख्या 1 देते हैं और अन्य प्रतिस्थापियों को इस प्रकार से संख्या देते हैं कि उनकी स्थितियों का योग न्यूनतम हो ।
संरचना एवं बन्धन (Structure and Bonding ) कार्बोक्सिलिक अम्ल में संरचना एवं बंधन को समझने के लिए फॉर्मिक अम्ल का उदाहरण लेते इसका एक कार्बन – ऑक्सीजन बंध दूसरे कार्बन – ऑक्सीजन बंध की अपेक्षा काफी छोटा है। इसमें हैं। इसमें –COOH समूह के कार्बन परमाणु की sp2 संकरित अवस्था है। यह एक समतलीय अणु है। बंध कोण लगभग 120° के होते हैं। इससे ऐसा लगता है कि इसमें 0+ कार्बन-ऑक्सीजन बंध (C = 0) ऐल्डिहाइड एवं कीटोन के कार्बोनिल समूह (>C = O) के अनुरूप है। हाइड्रॉक्सिल समूह का ऑक्सीजन परमाणु sp’ संकरित है। इस ऑक्सीजन परमाणु का एक एकाकी इलेक्ट्रॉन युग्म कार्बोनिल समूह के – निकाय के साथ कक्षक अतिव्यापन द्वारा अस्थानीकृत हो जाता है। हाइड्रॉक्सिल समूह के O- परमाणु के एकाकी इलेक्ट्रॉन युग्म का कार्बोनिल समूह के साथ संयुग्मन निम्नलिखित अनुनादी संरचनाओं क द्वारा प्रदर्शित कर सकते हैं-
हाइड्रॉक्सिल समूह द्वारा कार्बोनिल समूह को एकाकी इलेक्ट्रॉन युग्म प्रदान करने के कारण • कार्बोनिल समूह का इलेक्ट्रॉन स्नेही गुण ऐल्डिहाइड एवं कीटोन की अपेक्षा कम हो जाता है। कार्बोक्सिलिक अम्ल धुव्रीय होते हैं। एथेनोइक अम्ल, प्रोपेनोइक अम्ल तथा बेंजोइक अम्ल के द्विध्रुव आघूर्ण का मान 1.7 D से 1.9 D के मध्य होता है ।
भौतिक गुण (Physical Properties)
1. भौतिक अवस्था- C1-C9 के ऐलिफैटिक अम्ल द्रव हैं जबकि इससे ऊपर के मोम के समान रंगहीन ठोस हैं।
अधिकांश ऐरोमैटिक कार्बोक्सिलिक अम्ल रंगहीन क्रिस्टलीय ठोस पदार्थ हैं।
2. जल में विलेयता – C1 – C4 तक के ऐलिफैटिक अम्ल जल में पूर्णतया विलेय है परन्तु इसके बाद ऐल्किल समूह का आकार (हाइड्रोकार्बन भाग) बढ़ने के कारण जल में विलेयता तेजी से घटती है। ऐरोमैटिक अम्ल जल में अविलेय हैं। बेंजोइक अम्ल गर्म जल में घुल जाता है।
3. क्वथनांक एवं गलनांक- अणु भार में वृद्धि के साथ इनके क्वथनांक बढ़ते है । साधारणतया कार्बोक्सिलिक अम्लों के क्वथनांक उच्च होते हैं क्योंकि ये अन्तराअणुक हाइड्रोजन बंध द्वारा द्विलक बना लेते हैं।
ऐल्कोनोइक अम्लों की सजातीय श्रेणी के प्रथम दस सदस्यों के गलनांको में एक दूसरे सदस्य में एकान्तरण (Alternation) होता है, अर्थात् C-परमाणुओं की सम संख्या वाले एक अम्ल का गलनांक अपने से तुरन्त ऊपर तथा नीचे विषम संख्या C- परमाणु युक्त अम्लों से अधिक होता है (चित्र 6.1) 1
समसंख्या युक्त अम्ल में सिरे वाले मेथिल समूह एवं कार्बोक्सिलिक समूह, C- परमाणुओं की श्रृंखला पर एक दूसरे से विपरीत दिशा में होते हैं। इसलिए क्रिस्टल जाल में ठीक से समायोजित हो जाते हैं जिससे अन्तराअणुक आकर्षण बल प्रबल हो जाते हैं। विषम संख्या युक्त अम्ल में मेथिल समूह एवं कार्बोक्सिलिक समूह एक ही दिशा में होते हैं अतः अणु अपेक्षाकृत असममित हो जाता है जिसके कारण अन्तराअणुक आकर्षण अपेक्षाकृत कम हो जाते हैं और गलनांक कम हो जाता है ।
कार्बोक्सिलिक अम्लों की अम्लीय प्रकृति (Acidic Nature of Carboxylic Group )
कार्बोक्सिलिक समूह की संरचना (I) साधारणतया निम्न प्रकार लिखी जाती है:
कार्बोनिल ऑक्सीजन की विद्युतॠणता कार्बन से अधिक होने के कारण – C = O बन्ध के इलेक्ट्रॉन ऑक्सीजन की ओर विस्थापित हो जाते हैं जिससे कार्बन परमाणु पर धनावेश आ जाता है। अब C=O समूह के ध्रुवीय होने पर संरचना (I) को निम्न प्रकार संरचना (II) द्वारा प्रदर्शित किया जा सकता है-
संरचना (II) में कार्बन परमाणु इलेक्ट्रॉन न्यून हो जाता है जो हॉइड्रॉक्सिल समूह के ऑक्सीजन परमाणु पर उपस्थित एकाकी इलेक्ट्रॉन युग्म को अपनी ओर आकर्षित कर लेता है जिससे हाइड्रॉक्सिल समूह के ऑक्सीजन परमाणु पर इलेक्ट्रॉन की कमी हो जाती है। अब यह इलेक्ट्रॉन न्यून ऑक्सीजन, OH बन्ध के इलेक्ट्रॉनों को अपनी ओर आकर्षित कर लेता है तथा हाइड्रोजन परमाणु को प्रोटॉन (H+) के रूप में मुक्त कर देता है। इसलिए कार्बोक्सिल समूह अम्लीय प्रकृति दर्शाता है। इस सम्पूर्ण प्रक्रिया को निम्न प्रकार प्रदर्शित कर सकते हैं-
कार्बोक्सिल समूह की अम्ल प्रबलता को केवल उपर्युक्त कारण द्वारा नहीं समझाया जा सकता वरन् इसे कार्बोक्सिलिक समूह की अनुनादी संरचनाओं के द्वारा भी भली प्रकार समझाया जा सकता है। इस अनुनादी संरचाओं को निम्न प्रकार प्रदर्शित किया जा सकता है-
संरचना (VI) में हाइड्रॉक्सिल समूह के ऑक्सीजन पर धनावेश होने के कारण इसमें से प्रोटॉन सुगमता से निकल सकता है। जब कार्बोक्सिलिक अम्ल को विलायक जल में घोला जाता है तो यह आयनित होकर जल को प्रोटॉन दे देता है और संयुग्मी क्षार कार्बोक्सिलेट आयन (R-COO ) बनाता है। यह कार्बोक्सिलेट ऋणायन निम्नलिखित दो समान अनुनादी संरचनाओं (VII) और (VIII) द्वारा स्थायी हो जाता है।
कार्बोक्सिलेट ऋणायन की अनुनादी संरचनाओं (VII) और (VIII) में केवल ऋणावेश का ही अलगाव होता है। अतः इसकी अनुनादी ऊर्जा अनआयनित अम्ल की अनुनादी ऊर्जा से अधिक होती है, क्योंकि अनआयनित अम्ल की अनुनादी संरचनाओं (V) और (VI) में विपरीत आवेशों का अलगाव (Separation) होता है। इस प्रकार कार्बोक्सिलेट आयन की आन्तरिक ऊर्जा अनआयनित अम्ल से कम होती है, फलस्वरूप कार्बोक्सिलेट आयन अनआयनित अम्ल की अपेक्षा अधिक स्थायी होता है। इसलिये कार्बोक्सिलिक अम्ल से प्रोटॉन सुगमता से पृथक हो जाता है और इनको अम्लीय गुण प्रदान करता है। कार्बोक्सिलेट आयन और कार्बोक्सिलिक अम्ल के अनुनादी संकर (Resonance hybrid) को क्रमशः संरचना (IX) और (X) द्वारा प्रदर्शित किया जा सकता है।
समूह में C=0 द्विबन्ध और C-O एकल बन्ध की लम्बाई क्रमशः 1.23Á और 1.43 होनी चाहिए (क्योंकि कार्बोनिल यौगिकों में C=0 बन्ध की बन्ध लम्बाई 1.25 A और ईथर अथवा ऐल्कोहॉल में C–0 बन्ध की बन्ध लम्बाई 1.43À होती है, परन्तु –
में दोनों C= O बन्ध की बन्ध लम्बाई 1.28 À है। अतः यह कहा जा सकता है कि कर्बोक्सिलेट आयन और कार्बोक्सिलिक अम्ल के अनुनादी संकर लगभग क्रमशः उपर्युक्त संरचनाओं (IX) और (X) के द्वारा प्रदर्शित किये जा सकते हैं। अम्ल की संरचना (X) से स्पष्ट है कि इसमें कार्बोनिल समूह (> C=0) स्वतन्त्र रूप से उपलब्ध नहीं रहता है। अतः ऐल्कोनोइक अम्ल कार्बोनिल समूह की अभिक्रियाएं नही देते हैं।
कार्बोक्सिलिक अम्ल की अम्ल सामर्थ्य पर प्रतिस्थापियों का प्रभाव (Effect of Substituents on Acidic strength of Carboxylic Acids) ऐल्केनोइक अम्ल की अम्ल सामर्थ्य उसके आयनन पर निर्भर करती है। जैसा कि ऐल्केनोइक अम्ल की संरचना (X) का आयनन निम्न प्रकार दिखाया जा सकता है।
यदि अम्ल में ऐसा प्रतिस्थापी समूह अथवा परमाणु उपस्थित हो जो कार्बोक्सिलेट आयन (IX) को स्थायित्व प्रदान करे तो अम्ल (X) का आयनन बढ़ जायेगा और अम्ल सामर्थ्य बढ़ जायेगी। सामान्यतः इलेक्ट्रॉन आकर्षी समूह अथवा परमाणु (जैसे- हैलोजन, नाइट्रो, आदि)- I प्रभाव के कारण कार्बोक्सिलेट आयन के ऋणावेश को फैला देते हैं और ऋणायन का स्थायित्व बढ़ जाता है, जबकि इलेक्ट्रॉन प्रतिकर्षी अथवा इलेक्ट्रॉन मुक्त करने वाले समूह (जैसे- ऐल्किल) कार्बोक्सिलेट आयन के ऋणावेश में वृद्धि करके उसे अस्थाई कर देते हैं और अम्ल सामर्थ्य कम हो जाती है।
Z= इलेक्ट्रॉन आकर्षी (-1) समूह होने पर कार्बोक्सिलेट आयन पर ऋणावेश का फैलाव हो जाता है और इसका स्थायित्व बढ़ने के कारण अम्ल सामर्थ्यता बढ़ जाती है।
Z = इलेक्ट्रॉन प्रतिकर्षी (+I) समूह होने पर कार्बोक्सिलेट आयन पर ऋणावेश बढ़ता है। अतः इसका स्थायित्व कम होता है और अम्ल सामर्थ्यता घटती है।
समूह से हाइड्रोजन परमाणु
बंधित है जबकि अन्य ऐल्केनोइक अम्लों में ऐल्किल समूह जुड़ा होता है। अतः ऐल्किल समूह का +1 प्रभाव होने के कारण यह कार्बोक्सिलेट आयन पर ऋणावेश बढ़ा देता है जिससे उनके कार्बोक्सिलेट आयनों का स्थायित्व कम हो जाता है, परिणामस्वरूप अन्य ऐल्केनोइक अम्लो का आयनन कम होता है और मेथेनोइक अम्ल की अपेक्षा प्रोटॉन सुगमता से मुक्त नहीं हो पाते अतः अम्ल सामर्थ्यता कम हो जाती है। यहाँ यह बात ध्यान देने योग्य है कि पर अम्ल सामर्थ्यता कम हो जाती है।
इसी प्रकार यदि एथेनोइक अम्ल और 2-क्लोरो एथेनोइक अम्ल के अम्ल सामर्थ्य की तुलना करें तो 2-क्लोरो एथेनोइक अम्ल में क्लोरीन का (- 1) प्रभाव होने के कारण यह कार्बोक्सिलेट आयन के ऋणावेश का फैलाव कर देता है जिससे उसका स्थायित्व बढ़ जाता है। फलतः 2-क्लोरो एथेनोइक अम्ल का आयनन बढ़ जाता है जिससे प्रोटॉन एथेनोइक अम्ल की अपेक्षा सुगमता से प्राप्त हो जाते हैं। यह बात विशेष ध्यान देने योग्य है कि Z का (-I) प्रभाव बढ़ने पर अम्ल सामर्थ्यता बढ़ती है ।
कार्बोक्सिलिक अम्ल जल में प्रोटोन (H) देते हैं किन्तु H जल में H3O आयन के रूप में उपस्थित होता है। अतः वे यौगिक जो जल में आयनित होकर अधिक मात्रा में H® देते हैं (जो HO® आयन के रूप में उपस्थित रहता है) प्रबल अम्ल कहलाते हैं एवं दुर्बल अम्ल वे होते हैं जिनके आयनन से H® आयन बहुत कम मात्रा में प्राप्त होते हैं।
जल की मात्रा अम्ल की तुलना में बहुत अधिक होने के कारण उपर्युक्त समीकरण में इसको अपरिवर्ती (Constant) माना गया है। किसी अम्ल का वियोजन स्थिरांक (Ka) का मान यदि अधिक हो तो वह प्रबल अम्ल कहलाता है और इसका मान यदि कम है तो दुर्बल अम्ल कहलाता है। साधारणतया प्रबल एवं दुर्बल अम्ल की सामर्थ्य को उनके pKa मान में प्रदर्शित किया जाता है ।
pKa = -log Ka
प्रबल अम्ल में Ka का मान अधिक होता है जबकि pK काम मान कम होता है ।
कुछ अम्लों के Ka और pKa के मान निम्न सारणी 6.2 में दिए गये हैं-
हिंदी माध्यम नोट्स
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi sociology physics physical education maths english economics geography History
chemistry business studies biology accountancy political science
Class 12
Hindi physics physical education maths english economics
chemistry business studies biology accountancy Political science History sociology
English medium Notes
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi physics physical education maths entrepreneurship english economics
chemistry business studies biology accountancy
Class 12
Hindi physics physical education maths entrepreneurship english economics