actinometer in hindi types measures एनीमोमीटर क्या है क्या मापता है प्रकार उदाहरण
एनीमोमीटर क्या है क्या मापता है प्रकार उदाहरण actinometer in hindi types measures ?
प्रकाश के अवशोषित आइन्सटाइनों की संख्या या फोटॉनों की संख्या या प्रकाश तीव्रता का निर्धारण (Determination of Number of Einstein’s of light absorbed or Number of Photons absorbed or light intensity)
अवशोषित आइन्सटाइनों या फोटानों की संख्या या प्रकाश तीव्रता का निर्धारण थर्मोपाइल (Thermopile), फोटो इलेक्ट्रीक सैल या रासायनिक एक्टिनोमीटर द्वारा ज्ञात करते हैं।
(1) थर्मोपाइल (Thermopile)– ताप वैद्युत पाइल द्वारा प्रकाश तीव्रता का निर्धारण कर सकते हैं। पाइल में भिन्न
भिन्न धातुओं जैसे बिस्मथ तथा चाँदी की संधियों को एकान्तर श्रेणी में जोड़कर इस श्रेणी को एक गेल्वेनोमीटर से जोड़ देते हैं। संधि के एक छोर को काजल (lamp black) से काला कर देते हैं। पाईल की संधियों को प्रकाश से उद्भासित करने पर वे ऊर्जा का अवशोषण कर गर्म हो जाती है व ताप बढ़ जाता है जिससे गेल्वेनोमीटर में विक्षेप प्राप्त होता है जो प्रयुक्त प्रकाश की तीव्रता के संगत ही होता है। (चित्र 7.4 ) । पाइल को पहले से ही निश्चित प्रकाश भेजकर अंशाकित (Calibrate) कर लेते हैं। (चित्र 7.4)।
2. प्रकाश वैद्युत सैल (Photoelectric)
cell )- प्रकाश की तीव्रता का निर्धारण प्रकाश वैद्युत सैल द्वारा भी करते हैं (चित्र 7.5 ) । जब पराबैंगनी प्रकाश सक्रिय धातु इलेक्ट्रोड जैसे सीजीयम, पोटैशियम या सोडियम पर गिरता है तो धातुओं में से इलेक्ट्रॉनों को उत्सर्जित करता है। इसके परिणाम स्वरूप शेष धात्विक परमाणु धनात्मक हो जाते हैं। इलेक्ट्रॉनों के उत्सर्जन का वेग एमीटर में परिवर्तित विद्युत धारा द्वारा नाप लेते हैं। यह विद्युत धारा विकिरण की तीव्रता के समानुपाती होती है।
3. रासायनिक एक्टिनोमीटर द्वारा (By Chemical Actinometer)
इस विधि में किसी प्रकाश सुग्राही पदार्थ का चयन करके उसके विलयन में से प्रकाश को एक निश्चित समय के लिए गुजारा जाता है। प्रकाश गुजरने के पूर्व व बाद में पदार्थ का निर्धारण किसी भौतिक या रासायनिक (अनुमापन. चालकता, विभवमापी, आदि) द्वारा कर लेते हैं। पदार्थ की अपघटित मात्रा से प्रकाश की तीव्रता का निर्धारण कर लिया जाता है। इसमें प्रयुक्त प्रकाश सुग्राही पदार्थ को रासायनिक ऐक्टीनोमीटर तथा प्रक्रम को ऐक्टिनोमीटरी (actinometery) कहते हैं। उदाहरणार्थ-यूरेनिल आक्सलेट ऐक्टिनोमीटर।
यूरेनिल ऑक्सलेट ऐक्टीनोमीटर ऑक्सेलिक यूरेनिल ऑक्सलेट एक्टीनोमीटर में ऑक्सलिक अम्ल जो कि यूरेनिल आयन का सुग्राही है का अपघटन होता है। इस एक्टनीनोमीटर में 0.05 M ऑक्सेलिक अम्ल एवं 0.01M यूरेनिल सल्फेट का जलीय विलयन लेते हैं इस विलयन पर 250nm से 440 nm परास का पराबैंगनी प्रकाश गिराया जाता है। उत्तेजित UO2 2 + आयन अवशोषित ऊर्जा को
विलयन में अपघटित ऑक्सेलिक अम्ल की मात्रा का निर्धारण विलयन को प्रकाश से उद्भाषित करने से पूर्व व बाद में KMnO4 से अनुमापन कर ज्ञात कर लेते हैं। परमैंग्नेट आयन यूरेनिल आयन को प्रभावित नहीं करते। इस अभिक्रिया की क्वांटम दक्षता (लब्धि) 0.57 है। अतः इस अपघटित आक्सेलिक अम्ल की मात्रा से अवशोषित फोटान की संख्या या प्रकाश की तीव्रता की गणना कर सकते हैं।
सभी प्रयोगों में एक वर्णी (monochromatic) प्रकाश ही प्रयुक्त करना चाहिए अतः इसके लिए मोनो क्रोमेटर का उपयोग करते हैं।
आजकल यूरेनिल एक्टिनोमीटर के अलावा अन्य ऐक्टीनोमीटर जैसे फेरिआक्सलेट, रेनी लवण, एबरक्रोम (एक्टिनोमीटर) आदि का भी उपयोग करते हैं।
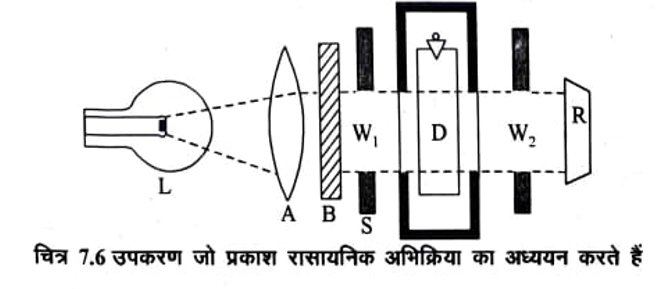
प्रकाश रासायनिक अभिक्रिया की प्रायोगिक व्यवस्था
चित्र 7.6 में दिखाये अनुसार L मरकरी वाष्प लैम्प या टंगस्टन लैम्प है जो प्रकाश का स्रोत है। इसमें से प्रकाश लैंस A द्वारा मोनोक्रोमेटर B में गुजरकर स्लिट S द्वारा अभिक्रिया सैल D जिसमें विलायक का विलयन है में खिड़की W से गिरता है तथा खिड़की W2 द्वारा रिकार्डर द्वारा मापन कर लेते हैं। बाद में सैल को क्रियाकारी पदार्थ के विलयन से भरकर उतने ही समय तक प्रकाश को भेजते हैं व R द्वारा मापन कर लेते हैं। इन दोनों अवस्थाओं में प्राप्त प्रकाश की तीव्रता का अन्तर ही अवशोषित प्रकाश की तीव्रता होती है।
क्वांटम दक्षता को प्रभावित करने वाले कारक (Factor Affecting Quantum Vield)
(1) ताप का प्रभाव: ताप के बढ़ाने पर क्वांटम दक्षता में थोड़ी वृद्धि होती है। उदाहरणार्थ अमोनिया की अपघटन की क्वांटम दक्षता 100°C बढ़ाने पर लगभग 15-20% बढ़ जाती है।
(2) तरंगदैर्घ्य का प्रभाव साधारणतया तरंगदैर्घ्य के बढ़ने पर क्वांटम दक्षता में कमी आती है।
(3) प्रकाश की तीव्रता का प्रभाव- प्रकाश की तीव्रता बढ़ाने पर क्वांटम दक्षता घट जाती है।
(4) निष्क्रिय गैसों का प्रभाव निष्क्रिय गैसों की उपस्थिति में साधारणतया प्रकाश रासायनिक अभिक्रिया की क्वांटम दक्षता में वृद्धि होती है। अतः प्रकाश रासायनिक अभिक्रिया में ताप स्थिर रहना चाहिए व एकवर्णी प्रकाश का उपयोग करना चाहिए।
विकिरण संक्रमण ( उत्सर्जन) (Radiative Transitions)
प्रतिदीप्ती या फ्लुओरेसेन्स (Fluorescence)
वे संक्रमण जिनमें सक्रियत अणु एकक उत्तेजित अवस्था S तथा त्रिक उत्तेजित अवस्था T1 से मूल एकक अवस्था Sg में आता है। इस संक्रमण में ऊर्जा का उत्सर्जन विकिरण के रूप में होता है। यदि अणु SI अवस्था से सीधा मूल एकक अवस्था (So) में लौट आता है वो प्रतिदीप्ती (fluorescence) उत्सर्जन होता है। यह लगभग 10-8 सेकिण्ड में होता है। इस संक्रमण में उत्सर्जित विकिरण को प्रतिदीप्ती कहते हैं।
अतः एक जैसी बहुलता अवस्था (like multiplicity states) में विकिरण संक्रमण अर्थात् एक उत्तेजित अवस्था से मूल एकक अवस्था में विकिरण के रूप में होता है। यदि अणु S, अवस्था से सीधा मूल एकक अवस्था (So) में लौट आता है वे प्रतिदीप्ती (Fluorescence) उत्सर्जन होता है। यह लगभग 10-85 में होता है। इस संक्रमण में उत्सर्जित विकिरण को प्रतिदीप्ती कहते हैं ।
अतः एक जैसी बहुलता अवस्था (like multiplicity states) में विकिरण संक्रमण अर्थात् एकक उत्तेजित अवस्था में मूल एकक अवस्था में विकिरण का उत्सर्जन प्रतिदीप्ती (Fluorescence) कहलाता है। इसका जीवन काल बहुत कम होता है अतः स्रोत के बन्द कर देने पर विकिरण उत्सर्जन तुरन्त बन्द हो जाता है। (चित्र 7.2 )
स्फुरदीप्ति या फोस्फोरेसेन्स (Phosphorescence)
इसी प्रकार संक्रमण ISC द्वारा S से T में जाकर T त्रिक उत्तेजित अवस्था से मूल एकक अवस्था Sg में लौटता है तो ऊर्जा का उत्सर्जन विकिरण के माध्यम से होता है इसको स्फुरदीप्ती (Phosphorescence) उत्सर्जन कहते हैं।
अतः अलग बहुलता अवस्था ( different multiplicity state) में विकिरण संक्रमण अर्थात् त्रिक उत्तेजित अवस्था (triplet state T) से मूल एकक अवस्था (So) में विकिरण का उत्सर्जन स्फुरदीप्तिी (Phosphorescence) कहलाता है। (चित्र 7.2) इसका जीवनकाल 10-3 सेकिण्ड या अधिक होता है अर्थात् विकिरण उर्त्सजन धीरे धीरे होता रहता है। प्रकाश स्रोत के बन्द कर देने पर भी कुछ देर तक उत्सर्जन होता रहता है।
प्रतिदीप्ती व स्फुरदीप्ती दोनों विकिरणों की आवृत्ति (उत्तेजित), उदभाषित प्रकाश (excited light) की आवृत्ति से कम होती है।
सामान्यतया T1 अवस्था का जीवनकाल S से अधिक होता है क्योंकि T की ऊर्जा S1 से कम होती है। अतः उत्तेजित अणु A की T अवस्था में रहने की प्रायिकता अधिक होती है। अतः अणु T अवस्था में आ जाता है क्योंकि यहां पर इसका जीवनकाल अपेक्षाकृत अधिक होता है। रासायनिक क्रिया कर उत्पाद बनाने का प्रक्रम यहां सम्पन्न होता है। अधिकांश प्रकाश रासायनिक क्रियाऐं इसी अवस्था में होती है।
क्वांटम लब्धि या क्वांटम दक्षता (Quantum Vield or Quantum Efficiency)
प्रकाश रासायनिक तुल्यता का नियम केवल अवशोषण या प्राथमिक रासायनिक प्रक्रम के लिए ही प्रयुक्त होता है। अर्थात् इसमें उत्पाद आगे और कोई अभिक्रिया नहीं करते हैं। जब प्रकाश का अवशोषण होता है तो पदार्थ का एक अणु एक फोटान का अवशोषण कर अपघटित भी हो जाये और अपघटित उत्पाद आगे कोई अभिक्रिया नहीं करे। ऐसी स्थिति में 11 का सम्बन्ध (एक अणु एक फोटान ) सही रूप से लागू होता है। लेकिन यदि प्राथमिक रासायनिक अभिक्रिया के साथ अन्य रासायनिक अभिक्रिया भी होती है जैसा कि श्रृंखला अभिक्रिया (H2 व Br2, H2 व Cl2 आदि) में होता है। एक फोटान के अवशोषण पर कई अणु अपघटित होते हैं तब 1 : 1 का सम्बन्ध सही रूप से लागू नहीं होता है अर्थात् रासायनिक तुल्यता का नियम 1: 1 सही नहीं है।
क्रिया करने वाले अणुओं की संख्या एवं अवशोषित फोटान की संख्या में सही सम्बन्ध ज्ञात करने के लिए एक नए पद की आवश्यकता हुई जो इसके साथ ही प्रकाश रासायनिक अभिक्रिया की क्रिया विधि तथा मात्रात्मक विश्लेषण को समझा सके। इस पद को क्वाटंम लब्धि या क्वाटंम दक्षता (Quantum yield or quantum efficiency) ¢ द्वारा प्रदर्शित किया गया।
किसी प्रकाश रायासनिक अभिक्रिया की क्वांटम दक्षता दिये गये समय में उत्पादों में रूपान्तरित होने वाले अणुओं की कुल संख्या तथा उसी समय में अवशोषित होने वाले फोटानो की कुल संख्या का अनुपात है।
दूसरे शब्दों में क्वाटं दक्षता या क्वाटंम लब्धि ($) प्रति फोटोन या क्वांटम प्रकाश अवशोषण से अभिक्रिया करने वाले क्रियाकारी अणुओं की संख्या है।
प्रकाश रासायनिक तुल्यता के नियमानुसार क्वाटंम दक्षता का मान हमेशा एक होना चाहिए लेकिन यह मान लगभग शून्य से लेकर 100 तक हो सकता है। (बहुत कम 0.04 से बहुत उच्च 106 तक हो सकता है)।
प्राथमिक प्रक्रम (चरण) के लिए क्वांटम लब्धि का मान हमेशा 1 होता है लेकिन जब द्वितीयक प्रक्रम (secondary process) होता है तब क्वांटम दक्षता का मान परिवर्तित होता है अर्थात् का मान प्राथमिक एवं द्वितीयक प्रक्रमों का समग्र परिणाम है और यह उस अभिक्रिया की प्रकृति पर निर्भर करेगा। अतः क्वांटम दक्षता को ज्ञात कर हम द्वितीयक प्रक्रम की प्रकृति को समझ सकते हैं।
क्वांटम लब्धि या दक्षता का प्रायोगिक निर्धारण (Experimental Determination of Quantum Yield or Efficiency)
किसी प्रकाश रासायनिक अभिक्रिया की क्वांटम दक्षता को निम्नलिखित व्यजंक द्वारा व्यक्त करते हैं।
अतः किसी प्रकाश रासायनिक अभिक्रिया के लिए क्वाटंम लब्धि के निर्धारण के लिए निम्न पदों का निर्धारण करते हैं।
(i) दिए गए समय में पदार्थ के अभिकृत हुए मोलों की संख्या
(i) उसी समय में निश्चित तरंगदैर्घ्य पर उसी पदार्थ द्वारा अवशोषित आइन्सटाइनों या फोटानों की संख्या या प्रकाश की तीव्रता का मापन ।
1. दिए गए समय में पदार्थ के अभिकृत हुए मोलों की संख्या दिए गए समय में रासायनिक बलगतिकी द्वारा ज्ञात कर लेते हैं क्योंकि यह अभिक्रिया की दर (वेग) है।
हिंदी माध्यम नोट्स
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi sociology physics physical education maths english economics geography History
chemistry business studies biology accountancy political science
Class 12
Hindi physics physical education maths english economics
chemistry business studies biology accountancy Political science History sociology
English medium Notes
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi physics physical education maths entrepreneurship english economics
chemistry business studies biology accountancy
Class 12
Hindi physics physical education maths entrepreneurship english economics