वाष्पदाब : वाष्पदाब अवनमन (△P) , राउल्ट का नियम , आदर्श विलयन (ideal solution) , वक्र , उदाहरण
राउल्ट का नियम
माना विलयन में दो वाष्पशील घटक A व B है। इन घटकों के आंशिक दाब क्रमशः PA
व PB है तथा इन घटकों मोल अंश XA
व XB है , तो राउल्ट के नियमानुसार –
PB = PB0XB
यहाँ PA = विलयन में उपस्थित A घटक का आंशिक दाब
PB = विलयन में उपस्थित B घटक का आंशिक दाब
PA0 = शुद्ध घटक A का वाष्पदाब
PB0 = शुद्ध घटक B का वाष्पदाब
वाष्पशील विलेय युक्त विलयन के लिए राउल्ट के नियम से कुल वाष्पदाब की गणना : यह द्रव-द्रव विलयन है। इसमें विलेय एवं विलायक दोनों घटक वाष्पशील है अत: विलयन का कुल वाष्पदाब इन दोनों घटकों के आंतरिक दाबो के योग के बराबर होगा।
माना विलयन में उपस्थित विलायक एवं विलेय घटक के आंशिक दाब क्रमशः
PA व PB है तथा इन घटकों मोल अंश XA व XB है , तो राउल्ट के नियमानुसार –
PB = PB0XB [समीकरण (2)]
यहाँ
PA0 = शुद्ध घटक A का वाष्पदाब
PB0 = शुद्ध घटक B का वाष्पदाब
अत: विलयन का कुल वाष्पदाब (P) = PA + PB [समीकरण (3)]
समीकरण-3 में समीकरण-1 तथा समीकरण-2 के मान रखने पर –
P = PA0 XA + PB0XB
चूँकि XA + XB = 1
XA = 1 – XBP = PA0 (1 – XB) + PB0XB
P = PA0 + XB ( PB0– PA0) [समीकरण (4)]
समीकरण-4 से विलयन का कुल वाष्पदाब ज्ञात कर सकते है।
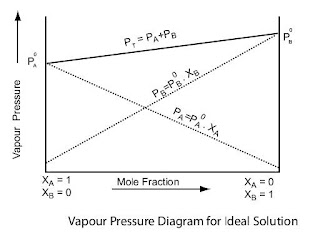
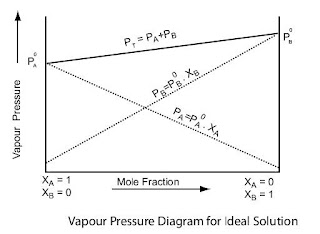
विलयन में उपस्थित विलेय एवं विलायक घटक के आंशिक दाब एवं उनके मोल अंश के मध्य वक्र सरल रेखा के रूप में प्राप्त होते है।
घटक A की तुलना में B घटक अधिक वाष्पशील है।
अवाष्पशील विलेय युक्त विलयन के लिए राउल्ट के नियम से कुल वाष्पदाब की गणना :
यह ठोस-द्रव विलयन है। इसमें विलेय ठोस अवाष्पशील है तथा विलायक द्रव वाष्पशील है अत: विलयन का कुल वाष्पदाब केवल विलायक के आंशिक दाब के बराबर होता है।
माना विलयन में विलायक घटक घटक A व विलेय घटक B हो तो राउल्ट के नियमानुसार –
PB = 0 [समीकरण (2)]
विलयन का कुल वाष्पदाब (P) = PA + PB
चूँकि PB = 0
(P) = PA [समीकरण (3)]
समीकरण-3 में समीकरण-1 का मान रखने पर –
P = PA0 XA
चूँकि XA + XB = 1
XA = 1 – XB
P = PA0 (1 – XB)
P = PA0 – PA0XB [समीकरण (4)]
समीकरण-4 से विलयन का कुल वाष्पदाब ज्ञात कर सकते है।
समीकरण-4 से –
PA0XB = PA0 – P
यहाँ PA0 – P वाष्पदाब अवनमन है।
XB = PA0 – P/PA0
[समीकरण (5)] में PA0 – P/PA0 वाष्पदाब का आपेक्षिक अवनमन है , ये विलेय की मोल भिन्न (XB) के बराबर होता है।
आदर्श विलयन (ideal solution)
अर्थात इन विलयनो का वाष्पदाब राउल्ट के नियम द्वारा ज्ञात किये गए वाष्पदाब के बराबर होता है।
[PA = PA0 XA]
[PB = PB0XB ]
[P = PA + PB]
ऐसे विलयन बनते समय न तो ऊष्मा का उत्सर्जन होता है और न ही अवशोषण होता है अर्थात इनमे एन्थैल्पी परिवर्तन का मान शून्य होता है।
△H = 0
ऐसे विलयन बनते समय विलयन का आयतन विलेय और विलायक के आयतन के योग के बराबर होता है अर्थात आयतन परिवर्तन का मान शून्य होता है।
△V = 0
इन विलयनो में AB अन्तरा आण्विक आकर्षण बल का परिमाण A-A आकर्षण बल व B-B आकर्षण बल के परिमाण के बराबर होता है।
A-B = A-A व B-B
A = विलायक के कण
B = विलेय के कण
आदर्श विलयन के लिए वक्र
हिंदी माध्यम नोट्स
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi sociology physics physical education maths english economics geography History
chemistry business studies biology accountancy political science
Class 12
Hindi physics physical education maths english economics
chemistry business studies biology accountancy Political science History sociology
English medium Notes
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi physics physical education maths entrepreneurship english economics
chemistry business studies biology accountancy
Class 12
Hindi physics physical education maths entrepreneurship english economics