u.v spectroscopy of enones in hindi यूवी स्पेक्ट्रोस्कोपी क्या है किसे कहते हैं उदाहरण सहित लिखिए
यूवी स्पेक्ट्रोस्कोपी क्या है किसे कहते हैं उदाहरण सहित लिखिए u.v spectroscopy of enones in hindi ?
फीजर-कॉहन नियम (Fischer – Kahn Rule )
यदि संयुग्मित तंत्र काफी बड़ा हो तो उसमें संक्रमण के लिये आवश्यक ऊर्जा का मान कम होगा। इस प्रकार के यौगिकों के λmax के मान को फ़ीजर कॉहन (Fischer – Kahn) के नियम द्वारा ज्ञात किया जाता है जिसे निम्नलिखित समीकरण के द्वारा देते हैं-
.λmax = 114 x 5M + n (48.0 – 1.7n ) – 16.5 R अन्तः
max = (1.74 x 104)n
जहां n = संयुग्मित द्विबंधों की संख्या
M= संयुग्मित तंत्र में ऐल्किल या ऐरिल समूहों की संख्या
R अन्तः = संयुग्मित तंत्र में अन्तः चक्रीय द्विबंध युक्त वलयों की संख्या
Rबाह्य = संयुग्मित तंत्र में बाह्य चक्रीय द्विबंध युक्त वलयों की संख्या
उदाहरण- 1 लाइकोपीन λmax में का मान ज्ञात करना ।
इस यौगिक में कुल संयुग्मित द्विबंधों की संख्या n = ।। है संयुग्मित तंत्र में छः मेथिल प्रतिस्थापी और दो ऐल्किल जैसे प्रतिस्थापी हैं जिन्हें बिंदुदार रेखा से दिखाया गया है। अतः M = 8
इस यौगिक में Rअन्तः तथा Rबाह्य की संख्या शून्य है।
फीजर कॉहन समीकरण प्रयुक्त करने पर
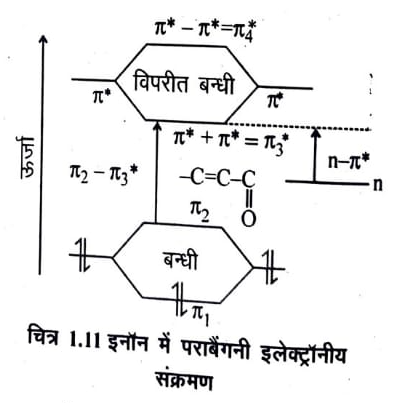
इनोन की U. V. स्पेक्ट्रोस्कोपी (U.V spectroscopy of enones) – a p – असंतृप्त कार्बोनिल यौगिकों को इनोन्स कहा जाता है। इन यौगिकों में दो प्रकार के इलेक्ट्रॉनीय संक्रमण पाये जाते हैं।
(i)>C=g:
इसमें प्रथम प्रकार का संक्रमण तीक्ष्ण (inntense) होता है तथा लघु तरंगदैर्ध्य प्रकाश की तरंगों के द्वारा सम्पन्न होता है जिसमें एक π इलेक्ट्रॉन विपरीत बन्धी π* कक्षक में विस्थापित हो जाता है। दूसरे प्रकार का संक्रमण (n -π *) संक्रमण है जिसमें ऑक्सीजन परमाणु का अबन्धी इलेक्ट्रॉन विपरीत बन्धी π*- कक्षक में विस्थापित हो जाता है। यह कम तीक्ष्ण (less intense) होता है क्योंकि यह उच्च तरंगदैर्ध्य के प्रकाश की तरंगों द्वारा सम्पन्न होता है। इसके द्वारा R-band का निर्माण होता है।
a. B-असंतृप्त कार्बोनिल यौगिकों में द्विबन्ध तथा कार्बोनिल समूह दोनों संयुग्मित अवस्था में होते हैं। यहाँ पर वर्णोंत्कर्षी विस्थापन होता है क्योंकि इलेक्ट्रॉन घनत्व कम से कम चार परमाणुओं (तीन C- परमाणु एवं एक O-परमाणु) पर विस्तारित हो जाता है। अतः a, B-असंतृप्त कार्बोनिल यौगिकों का U.V. स्पेक्ट्रम > CO समूह तथा ऐल्कीन समूह का योग होता है।
>C=O तथा >C=C< समूह संयुग्मन अवस्था में होने के कारण π- π* तथा n – π* दोनों प्रकार के संक्रमण पाये जाते हैं। उपर्युक्त ऊर्जा स्तर चित्र से यह सिद्ध होता है कि π2 (HOMO) ऊर्जा स्तर की ऊर्जा दोनों समूहों C=C एवं CO के π* ऊर्जा स्तरों की तुलना में अधिक होती है जबकि π3* (LUMO) ऊर्जा स्तर की ऊर्जा दोनों समूहों C = C एवं C = O के π* ऊर्जा स्तरों की तुलना में कम होती है। π2 – π3 * संक्रमण के लिए कम ऊर्जा की आवश्यकता होती है। अतः संक्रमण उच्च तरंगदैर्ध्य की परास वाली तरगों के द्वारा सम्पन्न होता है ।
275 से 300 nm क्षेत्र में एक वर्जित बैन्ड (Forbidden band) की उपस्थिति यौगिक में ऐल्डिहाइड तथा कीटोनिक समूह की उपस्थिति को दर्शाती है। यदि कोई ध्रुवीय समूह कार्बन परमाणु के साथ अक्षीय तथा भूमध्यीय अवस्था में जुड़ा हुआ है तो उसका अधिकतम अवशोषण तरंगदैर्घ्य निन्न प्रकार से प्रभावित होता है-
“अक्षीय अवस्था में जुड़े समूह के द्वारा λmax का मान अधिक वृद्धि करता है जबकि भूमध्यीय समूह के द्वारा कम विस्थापन होता है।”
π – π* तथा n – π* संक्रमणों की स्थिति उपयोग में लिए गये विलायक की प्रकृति पर भी निर्भर करती है। जैसे यदि विलायक की ध्रुवता (Polarity) बढ़ायी जाती है तो (π – π * ) संक्रमण में वर्णोत्कर्षी विस्थापन (Red shift) हो जाता है जबकि (π – π*) संक्रमण में वर्णोपकर्षी विस्थापन (blue shift) हो जाता है। ध्रुवीय विलायक संक्रमणों मे प्रयुक्त ऊर्जा स्तरों के ऊर्जा अन्तर को परिवर्तित कर देता है। यह विस्थापन आद्य अवस्था ऊर्जा स्तरों एवं उत्तेजित ऊर्जा स्तरों के स्थायित्व परिवर्तन के कारण होता है। (π – π*) संक्रमण में विलायक की ध्रुवणता बढ़ाने पर वणोपकर्षी विस्थापन विलायक तथा कार्बोनिल समूह के बीच हाइड्रोजन बन्ध बनने के कारण होता है। अतः हाइड्रोजन बन्ध के कारण अवशोषण निम्न तरंगदैर्घ्य की ओर विस्थापित हो जाता है चूंकि n ऊर्जा स्तर निम्न ऊर्जा की ओर विस्थापित हो जाता है ।
a,B–असंतृप्त कार्बोनिल यौगिकों (इनोनस) के लिए वुडवर्ड फ़ीजर नियम
वुडवर्ड फ़ीजर के द्वारा इनोनस के अधिकतम अवशोषण तरंगदैर्घ्य λmax का मान ज्ञात करने के लिए कुछ नियम दिये गये हैं जिन्हें बाद में स्कॉट ने परिवर्धित किया। ये नियम निम्न प्रकार हैं- (1) ac,B-असंतृप्त कीटानों के लिए मूल आधारीय मान 215nm लेते हैं। a, B-असंतृप्त कीटोन चक्रीय भी हो सकते हैं।
X
=CH-C= O यौगिक के लिए मूल मान 215 nm होता है जब X = ऐल्किल समूह हो। यदि X = H होतो मूल मान 207nm होगा। X = OH अथवा OR होने पर मूल मान 193 nm होगा ।
(2) यदि द्विबंध तथा कार्बोनिल समूह पांच सदस्यीय वलय के द्वारा जुड़े हो तो उसके लिए मूल मान 202 nm होगा ।
(3) विभिन्न प्रकार की संरचनाओं के द्वारा λmax के मान में होने वाली वृद्धि (Structural increments for estimating Amax for a given a, ẞ unsaturated carbonyl compound: Enones)
(i) प्रत्येक बाह्यचक्रीय द्विबन्ध के लिये = +5 nm
(ii) प्रत्येक पांच अथवा सात सदस्यीय वलय के अन्तः
चक्रीय द्विबंध युक्त यौगिकों में (साइक्लो- पेन्ट-2 ईनोन के अतिरिक्त) =+5nm
(iii) प्रत्येक ऐल्किल समूह तथा वलय अवशेष के लिए-
a- स्थिति पर = = + 10nm
B-स्थिति पर = + 12nm
Y अथवा 8 व उच्चतर स्थितियों पर = +18nm
(iv) प्रत्येक संयुग्मन विस्तार वाले द्विबन्ध के लिए = + 30nm
(v) समवलीय संयुग्मित डाइईन के लिए = 39 nm
(4) विभिन्न प्रकार के वर्णमूलकों के विभिन्न स्थितियों पर जुड़ने के कारण λmax के मान में होने वाली वृद्धि निम्नलिखित सारणी में दी गई है-
इन सभी मानों का उपयोग कर प्रत्येक इनोन के लिए λmax का मान ज्ञात किया जा सकता है।
उदाहरण 1:
हल : इसके लिये मूल मान = 215 nm
इसमें दो B- ऐल्किल समूह (2×12 ) के कारण λmax = 2 x 12 nm = 24 nm
अतः यौगिक के लिये λmax = 215 +24nm = 239 nm
उदाहरण 2.
हल : यदि किसी यौगिक में C= O बंन्ध के साथ क्रॉस संयुग्मन हो तो λmaxके मान का निर्धारण उस दिशा से करते हैं जिस दिशा की ओर संयुग्मित तन्त्र अधिक प्रतिस्थापित हो अर्थात अधिक समूह जुड़े हुए हों। अतः उपर्यक्त यौगिक में C समूह क्रॉस संयुग्मित है परन्तु C – वलय की और वह अधिक प्रतिस्थापित है। अतः λmax का निर्धारण C – वलय की ओर से करेंगे-
λmax का मान विलायक की प्रकृति पर निर्भर करता है क्योंकि n – π * संक्रमण का मान हाइड्रोजन बन्ध की उपस्थिति के कारण निम्न तरंगदैर्घ्य की ओर विस्थापित हो जाता है अर्थात (Blue shift) होती है क्योंकि प्रत्येक विलायक की ध्रुवता भिन्न होती है। अतः ज्ञात है कि ध्रुवता बढ़ने पर हाइड्रोजन बन्धुता बढ़ती है। प्रत्येक विलायक के द्वारा λmax में मान में होने वाला परिवर्तन निम्नानुसार होता है-
विशिष्ट क्रियात्मक समूह युक्त यौगिकों के UV स्पेक्ट्रम (UV spectrum of compounds having specific functional group) :-
1. कार्बोक्सिलिक अम्ल (Carboxylic acid):-
संतृप्त कार्बोक्सिलिक अम्ल में – COOH क्रियात्मक समूह होता है इसमें > C = 0 क्रोमोफोर के साथ – OH ऑक्सोक्रोम जुड़ा रहता है । – OH की उपस्थिति के कारण हिप्सोक्रोमिक शिफ्ट मिलती है तथा कार्बोक्सिलिक अम्ल लगभग 200 nm पर एक दुर्बल अवशोषण बैण्ड प्रदर्शित करते हैं। ऐल्किल समूह की श्रृंखला अथवा संख्या बढ़ने पर बैथोक्रोमिक शिफ्ट मिलती है जिससे max का मान बढ़ जाता है a p असंतृप्त अम्ल में π – π* संक्रमण भी मिलते हैं।
2. ऐरोमैटिक यौगिक (Aromatic compound) :-
बैजीन ऐरोमैटिक यौगिको की मूल इकाई है। इसमें π3 बन्ध होते हैं जिनके कारण π – π* संक्रमण मिलते हैं। बैंजीन निम्नलिखित तीन प्रकार के अवशोषण बैण्ड प्रदर्शित करता है।
(i) E1 बैण्ड :- यह 184 nm पर मिलता है जिसका Ema = . = 60,000 होता है।
(ii) E2 बैण्ड:- यह 204 nm पर दुर्बल बैण्ड के रूप में मिलता है इसका Emax = 7900 होता है।
(iii) B-बैण्ड :- यह 256 nm पर अत्यन्त दुर्बल बैण्ड के रूप में मिलता है इसका Emax = 200 होता है ।
(a) बैंजीन तथा उसके सजात की पहचान में B- बैण्ड महत्त्वपूर्ण होता है। ऐल्किल समूहों की संख्या बैजीन वलय पर बढ़ने से बैथोक्रमिक शिफ्ट मिलती है अर्थात् λmax में वृद्धि होती है। इसे सारणी 1.4 द्वारा समझा जा सकता है।
बैंजीन एवं उसके सजात में वाष्प अवस्था में अथवा अध्रुवीय विलायकों की उपस्थिति में सूक्ष्म संरचनात्मक बैण्ड प्राप्त होते हैं यह प्रभाव π – π* संक्रमण का अणुओं के कम्पन से अन्नोन्य क्रिया के कारण होता है जबकि ध्रुवीय विलायकों की उपस्थिति में यह प्रभाव कम अथवा समाप्त हो जाता है।
(b) बैंजीन में यदि ऑक्सोक्रोम (ÖH, ÖR, ŚR, NH,) जुड़ा हो तो अबन्धी इलेक्ट्रॉन की कारण बैथोक्रोमिक शिफ्ट मिलती है अर्थात् λmax में वृद्धि होती है इसे सारणी उपस्थिति 1.5 से समझा जा सकता है।
यदि ऐनिलीन के NH2 समूह पर उपस्थित एकाकी इलेक्ट्रॉन युग्म H+ को ग्रहण कर ऐनिलीनियम आयन (धनायन) बनाता है तो n – इलेक्ट्रॉन की अनुपलब्धता के कारण अवशोषण बैण्ड में हिप्सोक्रोमिक विस्थापन मिलता है। इसके विपरीत फीनॉल से एक प्रोटोन के निष्कासन पर फीनोलेट आयन (ऋणायन) बन जाने के कारण n-इलैक्ट्रोनों की उपलब्धता अनुनाद के लिए बढ़ जाती है जिसमें π – π* संक्रमण
आसान हो जाता है तथा बैथोक्रोमिक विस्थापन मिलता है। इसे सारणी 1.6 द्वारा समझा जा सकता है।
यदि बैंजीन वलय पर कोई असंतृप्त समूह अर्थात् क्रोमोफोर जुड़ा हो तो बैंजीन के B बैण्ड के mav में वृद्धि हो जाती है। ऐसा K बैण्ड (संयुग्मन बैण्ड) के कारण होता है। बैजीन वलय के इलेक्ट्रॉन तथा असंतृप्त समूह के इलेक्ट्रॉन संयुग्मन में होने के कारण बैथोक्रोमिक शिफ्ट मिलती है। कुछ ऐसे यौगिकों K बैण्ड तथा B बैण्ड सारणी 1.7 में दिए जा रहे हैं।
यदि एक ही वलय पर ऑक्सोक्रोम तथा क्रोमोफोर दोनों उपस्थित हो तो दोनों बैथोक्रोमिक शिफ्ट में योगदान देते हैं। यह प्रभाव p-समावयवी में सर्वाधिक होता है क्योंकि इसमें अनुनादी संरचनाएं बनती है p- नाइट्रोऐनिलीन तथा p- नाइट्रोफीनॉल की अनुनादी संरचनाऐं निम्नलिखित है।
o -तथा-समावयवियों की तुलना में p- समावयवियों के के मान सर्वाधिक होते हैं साथ ही इनमें ऐरोमैटिक तंत्र का B बैण्ड विलुप्त (Submarge) हो जाता है। नाइट्रोऐनिलीन तथा नाइट्रोफीनॉल के विभिन्न समावयवियों के K तथा B-बैण्ड सारणी 1.8 में दिए जा रहे हैं।
सारणी 1.8 नाइट्रोऐनिलीन तथा नाइट्रोफीनॉल के विभिनन समावयवियों के K तथा B- बैण्ड यौगिक संरचना K- बैण्ड
हिंदी माध्यम नोट्स
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi sociology physics physical education maths english economics geography History
chemistry business studies biology accountancy political science
Class 12
Hindi physics physical education maths english economics
chemistry business studies biology accountancy Political science History sociology
English medium Notes
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi physics physical education maths entrepreneurship english economics
chemistry business studies biology accountancy
Class 12
Hindi physics physical education maths entrepreneurship english economics