क्रिस्टल क्षेत्र विपाटन (crystal field splitting in hindi) क्रिस्टल क्षेत्र विभाजन ऊर्जा को प्रभावित करने वाले कारक crystal field split energy
क्रिस्टल क्षेत्र विपाटन (crystal field splitting in hindi) : क्रिस्टल क्षेत्र विभाजन ऊर्जा को प्रभावित करने वाले कारक crystal field split energy in hindi) , दो सेट में एक कक्षाओं के बंटवारे पर चर्चा एक क्रिस्टल क्षेत्र है और क्रिस्टल क्षेत्र में 1 अक्षरों का 2 समूह में विभाजित होने को समझाइए ?
crystal field split energy क्रिस्टल क्षेत्र विभाजन ऊर्जा : t2g एवं eg कक्षकों के मध्य के उर्जा अंतर को क्रिस्टल क्षेत्र विभाजन उर्जा कहते है।
क्रिस्टल क्षेत्र स्थायीकरण उर्जा (crystal field stabilization energy ) (CFSE) : d कक्षकों के उच्च उर्जा के eg एवं निम्न उर्जा के t2g कक्षकों में विभाजन के पश्चात् e के निम्न उर्जा स्तर में जाने की प्रवृति होती है इसलिए t2g कक्षकों में electron के प्रवेश करने से उर्जा मुक्त होती है एवं eg कक्षकों में e के प्रवेश करने से उर्जा अवशोषित होती है अत: इस प्रक्रिया के दौरान कुछ उर्जा निष्कासित होती है जिसे CFSE कहते है।
CFSE का मान तंत्र के स्थायित्व को दर्शाता है इसलिए इसका मान ऋणात्मक होता है।
धातु आयन के t2g एवं eg कक्षकों के e की संख्या के आधार पर CFSE का मान ज्ञात किया जाता है।
अष्ट फलकीय संकुलों के लिए CFSE का मान शून्य या ऋणात्मक हो सकता है लेकिन धनात्मक नहीं हो सकता।
प्रश्न : क्या कारण है की चतुष्फलकीय संकुल यौगिक सैदेव उच्च चक्रण संकुल यौगिक बनाते है।
उत्तर : चतुष्फलकीय संकुल यौगिकों क्रिस्टल क्षेत्र विभाजन उर्जा का मान प्रबल एवं दुर्बल क्षेत्र दोनों ही प्रकार के लिगेंड़ो के लिए कम होता है अत: इस दोनों ही electrons के लिए कम होता है , अत: इन दोनों electrons के लिए क्रिस्टल क्षेत्र उर्जा का मान pi उर्जा से कम होता है।
इसलिए e की युग्मन की सम्भावना नगण्य होती है , फलस्वरूप चतुष्फलकीय संकुल सैदेव उच्च चक्रण वाले होते है।
क्रिस्टल क्षेत्र विभाजन उर्जा को प्रभावित करने वाले कारक
1. धातु आयन की प्रकृति
2. लिगेण्ड की प्रकृति
3. लिगेण्ड का आकार
4. संकुल की ज्यामिति
क्रिस्टल क्षेत्र विपाटन (crystal field splitting) : अष्टफलकीय , चतुष्फलकीय और वर्ग समतल संकुलों में क्रिस्टल क्षेत्र विपाटन (crystal field splitting in octahedral tetrahedral and square planar complexes in hindi) : जब धातु परमाणु अथवा आयन अपनी निम्नतम ऊर्जा अवस्था में होता है तब पाँचो d कक्षक समान ऊर्जा वाले होते है परन्तु जैसे ही इस धातु परमाणु अथवा आयन के सम्पर्क में कोई लिगैण्ड आता है , इन पांचो कक्षकों का विभाजन अथवा विपाटन हो जाता है एवं किस प्रकार का संकुल बन रहा है , किस दिशा में लिगैंड धातु आयन के पास पहुँच रहा है , इस आधार पर कुछ कक्षक उच्च ऊर्जा स्तर में चले जाते है जबकि कुछ अन्य निम्न ऊर्जा स्तर पर चले जाते है। इसे क्रिस्टल क्षेत्र विपाटन कहते है।
1. अष्टफलकीय संकुलों में क्रिस्टल क्षेत्र विपाटन : जब कोई अष्टफलकीय संकुल बन रहा होता है तो छ: लिगैण्ड एक अष्टफलक के कोनों की ओर से अर्थात x , y और z अक्षों की ओर से केन्द्रीय धातु आयन की ओर पहुँच सकेंगे।
इस प्रकार जब अष्टफलकीय आकार में छ: लिगैण्ड केन्द्रीय धातु परमाणु की ओर पहुँचते है तो समस्त d कक्षकों की ऊर्जा के मान में वृद्धि हो जाती है लेकिन Eg (dx2-y2 और dz2) कक्षक जो कि x- , y- , z-अक्षों की ओर अभिविन्यासित होते है वे अधिक प्रतिकर्षित होने के कारण उच्च ऊर्जा स्तर पर चले जायेंगे और शेष तीनो कक्षक x- , y- , z- अक्ष रेखाओं के मध्य की ओर अभिविन्यासित होते है अर्थात t2g (dxy , dyz , dzx) कक्षक निम्न ऊर्जा स्तर पर चले जायेंगे। इस प्रकार eg और t2g कक्षकों में से eg कक्षक उच्च ऊर्जा स्तर पर चले जाते है जबकि t2g कक्षक निम्न ऊर्जा स्तर पर चले जाते है।
इन दोनों प्रकार के d कक्षकों की ऊर्जा का अंतर △0* (या 10 Dg) के रूप में प्रदर्शित किया जाता है। △0 अथवा 10Dq को क्रिस्टल क्षेत्र विपाटन ऊर्जा कहते है तथा उपर्युक्त से यह स्पष्ट होता है कि eg कक्षक औसत ऊर्जा स्तर से +0.6△0 ऊपर होते है जबकि t2g कक्षक औसत ऊर्जा स्तर से -0.4△0 नीचे होते है।
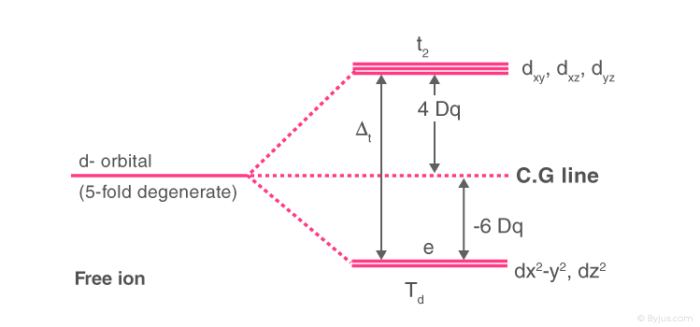
2. चतुष्फलकीय संकुलों में क्रिस्टल क्षेत्र विपाटन : एक नियमित चतुष्फलक एक घन से सम्बन्धित होता है जिसके केंद्र में धातु परमाणु होता है तथा आठ में से एकांतर चार कोनो पर लिगैण्ड उपस्थित रहते है।
स्पष्ट है कि x , y और z अक्ष घन के फलकों की ओर इंगित करते हुए है। पांचो d कक्षकों को उपर्युक्त प्रकार के घन के अक्षो के सन्दर्भ में देखने से स्पष्ट है कि यदि चतुष्फलकीय आकार में चार लिगैण्ड धातु आयन की ओर पहुंचेंगे तो वे eg और t2g कक्षकों में से किसी के भी एकदम सीध में नहीं होंगे। eg कक्षक , केन्द्रीय धातु आयन और लिगैंड के मध्य के कोण का मान 54.44′ होता है जबकि t2g कक्षक , केन्द्रीय धातु आयन और लिगैण्ड के मध्य के कोण का मान 35.16′ होता है अर्थात t2g कक्षक लिगैण्ड की दूरी eg कक्षक लिगैण्ड की दूरी से कम होती है।
जब लिगैंड केन्द्रीय धातु आयन की ओर पहुँचते है तो समस्त d कक्षकों की ऊर्जा के मान में वृद्धि हो जाती है लेकिन t2g कक्षकों के लिगैंड से अधिक निकट होने के कारण उनकी ऊर्जा अधिक हो जाती है। इस प्रकार चतुष्फलकीय क्षेत्र में d कक्षकों का क्रिस्टल क्षेत्र विभाजन अष्टफलकीय क्षेत्र की तुलना में एकदम विपरीत है | अत: गोल सममित क्षेत्र में d कक्षकों की औसत ऊर्जा की तुलना में t2g कक्षकों की ऊर्जा +0.4△t* उच्च होती है जबकि eg कक्षकों के लिए ऊर्जा का मान औसत ऊर्जा की तुलना में -0.6△t* कम होता है।
चतुष्फलकीय और अष्टफलकीय क्रिस्टल क्षेत्र विभाजन अथवा विपाटन की तुलना
- एक अष्टफलकीय क्षेत्र में छ: लिगैण्ड धातु की ओर पहुँचते है जबकि एक चतुष्फलकीय क्षेत्र में केवल चार ही लिगैण्ड केन्द्रीय धातु पर पहुंचेंगे अत: अष्टफलकीय क्षेत्र का विभाजन 2/3(4/6 = 2/3) ही होगा।
- अष्टफलकीय लिगैंड क्षेत्र में लिगैण्ड eg कक्षको के एकदम सीध में पहुँचते है जिससे प्रतिकर्षण अधिक होता है जिससे क्रिस्टल क्षेत्र विभाजन भी अधिक होगा। इसके विपरीत , चतुष्फलकीय क्षेत्र में लिगैण्ड किसी भी कक्षक के एकदम सीध में नहीं होते जिसके फलस्वरूप प्रतिकर्षण कम होता है तथा इस कारक की वजह से भी क्रिस्टल क्षेत्र विभाजन लगभग 2/3 रह जाता है।
अत:कुल मिलाकर अष्टफलकीय लिगैण्ड क्षेत्र विभाजन △0 की तुलना में चतुष्फलकीय लिगैण्ड क्षेत्र विभाजन △t का मान लगभग 4/9 हो जाता है , अर्थात
- चार बन्धो की तुलना में छ: बंध बनने में अधिक ऊर्जा मुक्त होती है , अत: अष्टफलकीय संकुल स्थायी होते है।
- चतुष्फलकीय क्षेत्र की तुलना में अष्टफलकीय क्षेत्र के लिए CFSE का मान अधिक होता है।