वास्तविक गैसों के आदर्श व्यवहार से विचलन , क्यों वास्तविक गैस आदर्श व्यवहार से विचलित होती है
क्यों वास्तविक गैस आदर्श व्यवहार से विचलित होती है वास्तविक गैसों के आदर्श व्यवहार से विचलन को संक्षेप में समझाइए DEVIATION FROM IDEAL GAS BEHAVIOUR in hindi ?
वास्तविक गैसें (Real Gases)
समस्त गैसें निम्न दाब और उच्च ताप पर तो आदर्श व्यवहार करती हैं, किन्तु निम्न ताप व उच्च दाब पर उनका आचरण आदर्श गैसों से बहत विचलित हो जाता है। ऐसी सब गैसें वास्तविक गैसें (real cases) कहलाती हैं। कोई भी गैस पूर्णतः आदर्श गैस नहीं हो सकती। ताप व दाब की परिस्थितियों में गैसों का आचरण वास्तविक अथवा आदर्श होता है।
आदर्श गैस आचरण से विचलन (DEVIATION FROM IDEAL GAS BEHAVIOUR)
अपने सरलतम रूप में PV = RT एक आदर्श गैस समीकरण है जो गैसों की निश्चित मात्रा (1 मोल) के लिए ताप, दाब व आयतन में सम्बन्ध दर्शाती है। एक आदर्श गैस के लिए PV व्यंजक का मान प्रत्येक ताप व दाब पर एक (one) होना चाहिए, अर्थात् PV / RT=1 PV/RT व्यंजक को हम संपीड्यता गुणांक (compressibility factor) कहते है और इसे 2 द्वारा प्रदर्शित करते हैं, अतः
Z = PV/RT
अर्थात किसी आदर्श गैस के लिए Z का मान सदैव । चाहिए। लेकिन वास्तव में शून्य दाब के अतिरिक्त की गैस का संपीड्यता व्यंजक 1 नहीं होता अर्थात शन्य सभी गैसें आदर्श व्यवहार करती हैं। कुछ गैसों के लिए, व्यंजक व दाब के मध्य खींचे गये वक्र उपर्युक्त चित्र दर्शाये गये हैं। इस प्रकार के वक्र सर्वप्रथम 1818 में (Amagat) ने खींचे थे, इसी से इन्हें अमेगट वक्र भी का अमेगट वक्र भी कहा जाता
वक्रों का आदर्श गैस के वक्र से नीचे जाना अर्थात व्यंजक का मान इकाई से कम होना यह दशाता है कि संपीड्यता आदर्श गैस से अधिक है। ऐसी गैसों को आसानी । चित्र 3.4.0C पर H2,02 तथा 40°C पर द्रवित किया जा सकता है।
हाइड्रोजन व हीलियम जैसी CO2 के लिए संपीड्यता व्यंजक व दाब जिनका क्वथनांक बहुत कम होता है, आदर्श गैस से अधिक संपीड्यता नहीं दर्शातीं, शून्य से बहुत नीचे वाले ताप पर खींचे गये वक्रों को छोड़कर सदैव इनके वक्र आदर्श गैस के ऊपर ही रहते हैं।
वक्रों का आदर्श गैस के ऊपर जाना उनकी घटती हुई संपीड्यता को दशाता ह, दाब इनकी संपीड्यता कम होती जाती है। हाइड्रोजन व हीलियम के अतिरिक्त समस्त गैसों के वक्र दाब बढ़ने के साथ पहले धीरे-धीरे नीचे की ओर आते हैं फिर तेजी से ऊपर की ओर बढ़ते हैं। इससे यह निष्कर्ष निकलता है कि प्रारम्भ में तो दाब बढ़ने से गैसों की संपीड्यता आदर्श गैस से अधिक होती है, किन्तु उच्च दाब पर इनकी संपीड्यता में तेजी से कमी आती है।
यदि किसी एक ही गैस के संपीड्यता व्यंजक के दाब के साथ अलग-अलग ताप पर वक्र खींचें, तो संलग्न प्रकार का चित्र प्राप्त होता है (चित्र 3.5)।
चित्र 3.5 से स्पष्ट है कि गैस का ताप जैसे-जैसे आदर्श गैस बढ़ता जाता है वक्र का ढाल (dip or downward slope) कम होता जाता है और वक्र आदर्श गैस के समीप आता जाता है। एथिलीन के लिए 624 K पर P(atm) लगभग 200 atm दाब तक वक्र आदर्श गैस के साथ चल रही है अर्थात् इस क्षेत्र में संपीड्यता व्यंजक Z चित्र 3.5. विभिन्न तापमानों पर एथिलीन गैस के लिए का मान लगभग एक है। दूसरे शब्दों में, इस ताप पर संपीड्यता Z व दाब P के मध्य वक्र (T = बॉयल का ताप) बॉयल के नियम का पालन हो रहा है। इस ताप को बॉयल ताप (Boyle’s temperature) कहा जाता है और इसे इस प्रकार परिभाषित किया जा सकता है-“वह ताप जिस पर शून्य से दाब के पर्याप्त क्षेत्र में कोई गैस बॉयल के नियम का पालन कर रही हो वह उस गैस का बॉयल ताप कहलाता है।” अत: एथिलीन का बॉयल ताप 624 K है।
इस प्रकार हम निष्कर्ष निकाल सकते है कि पर्याप्त ताप व कम दाब पर तो गैसों का व्यवहार आदर्श गैस के आस-पास रहता है, किन्तु कम ताप व अधिक दाब पर आदर्श गैस के व्यवहार से बहत अधिक विचलन हो जाता है, विशेष तौर से उच्च दाब पर तो यह विचलन बहुत ही स्पष्ट हो जाता है।
आदर्श आचरण से विचलन के कारण (CAUSES OF DEVIATIONS FROM IDEAL BEHAVIOUR)
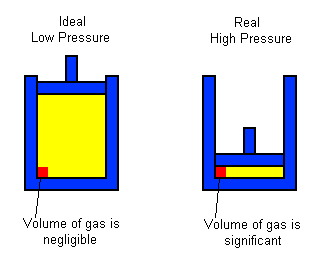
आदर्श गैस अथवा गैसों के आदर्श आचरण से तात्पर्य है कि समस्त गैस नियमों (बॉयल, चार्ल्स, गै-लूसाक, आदि) का पूर्णरूप से पालन करें। ये सभी नियम गैसों के अणुगति सिद्धान्त (kinetic theory of gases) पर आधारित हैं और गैसों का अणुगति सिद्धान्त कुछ आधारभुत कल्पनाओं या अवधारणाओ। postulates) पर आधारित है। यदि यथार्थ में गैसों का आचरण आदर्श गैस के समान नहीं है तो अवश्य हा दिन मल अवधारणाओं में कोई त्रुटि है। गैसो के अणगति सिद्धान्त की मल अवधारणाओं में निम्न दो। अवधारणाएं प्रमुख हैं (i) गैसों के अणु इतने छोटे होते हैं कि उनका आयतन गैस के कल आयतन की तुलना में नगण्य ना है। गैसों के आयतन का प्रमुख भाग वह रिक्त स्थान होता है जिसमें ये अणु स्वतन्त्रतापूर्वक विचरण हो । ताप व दाब की सामान्य परिस्थितियों में यह अवधारणा ठीक भी लगती है क्योंकि इस अवस्था गैस के अणुओं का आयतन गैस के कुल आयतन का लगभग 0.014% होता है। यह प्रतिशतता इतनी कम है कि हम इसका उपक्षा (negligence) कर सकते हैं इसीलिए ताप व दाब की सामान्य परिस्थितियों में औमें आदर्श आचरण करती भी है, विचलन तो उच्च दाब पर बढ़ता है। उच्च दाब पर गैसें संपीडित हो जाती हैं गैस अणओं के मध्य का रिक्त स्थान कम हो जाता है। जब अणओं के मध्य का रिक्त स्थान कम हो जायेगा को गैस अणुओं का आपेक्षिक आयतन बढ़ जायेगा अर्थात् गैस के कल आयतन की तुलना में गैस के अणुओं का आयतन अब उतना कम नही रहेगा जितना सामान्य परिस्थितियों में था। उदाहरण के लिए, यदि सामान्य रिस्थितियों में गैस अणुओं का आयतन गैस के कुल आयतन का 0.014% है तो दाब 100 गुना करने पर पर 14% हो जायेगा, दाब को 1000 गुणा करने पर यह 14% हो जायेगा। इस प्रकार गैस का दाब जैसे जैसे बढ़ता जायेगा कुल आयतन की तुलना में उनके अणओं का आपेक्षिक आयतन बढ़ता जायेगा और गैस अणुओं के इतने बढ़े हुए आयतन को उपेक्षित नहीं कर सकते। यही कारण है कि उच्च दाब पर गैसें आदर्श व्यवहार से अधिक विचलन दर्शाती हैं। (2) गैसों के अणुगति सिद्धान्त की दूसरी महत्वपूर्ण अवधारणा यह है कि गैसों के अणुओं के मध्य परस्पर कोई आकर्षण बल नहीं होता। यह बात भी सामान्य ताप व दाब पर तो ठीक लगती है, क्योंकि इन परिस्थितियों में अणुओं के मध्य इतना अधिक रिक्त स्थान होता है कि वे एक-दूसरे से बहुत दूर-दूर रहते हैं फलतः उनके मध्य कोई आकर्षण बल कार्यरत नहीं हो पाता। किन्तु निम्न ताप व उच्च दाब पर, जब गैस अणुओं के मध्य रिक्त स्थान कम हो जाता है और वे एक-दूसरे के नजदीक आ जाते हैं, तो ऐसी अवस्था में अणुओं के मध्य आकर्षण बल अवश्य रहेगा। इसके पक्ष में हम दो प्रमाण दे सकते हैं
- गैसों का द्रवीकरण (Liquifaction of gases)
यदि गैसों के अणुओं के मध्य कोई आकर्षण बल नहीं हो तो उनका द्रवीकरण करना सम्भव नहीं होता, जबकि अधिकांश गैसें निम्न ताप व उच्च दाब पर द्रवित हो जाती हैं।
हिंदी माध्यम नोट्स
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi sociology physics physical education maths english economics geography History
chemistry business studies biology accountancy political science
Class 12
Hindi physics physical education maths english economics
chemistry business studies biology accountancy Political science History sociology
English medium Notes
Class 6
Hindi social science science maths English
Class 7
Hindi social science science maths English
Class 8
Hindi social science science maths English
Class 9
Hindi social science science Maths English
Class 10
Hindi Social science science Maths English
Class 11
Hindi physics physical education maths entrepreneurship english economics
chemistry business studies biology accountancy
Class 12
Hindi physics physical education maths entrepreneurship english economics